题目内容
9.我国化学家侯德榜发明了联合制碱法,其生产工艺流程如图所示: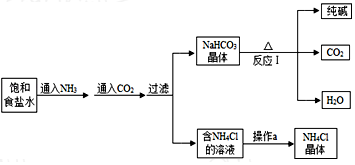
(1)纯碱溶液可以使无色酚酞试液变红色.
(2)写出反应I的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)操作a的过程是蒸发浓缩、降温结晶、过滤.
(4)上述工艺流程中可循环利用的物质是二氧化碳.
分析 (1)碳酸钠溶液显碱性,能使酚酞试液变红色;
(2)反应I中,碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;
(3)操作a的过程是蒸发浓缩、降温结晶、过滤;
(4)上述工艺流程中可循环利用的物质是二氧化碳.
解答 解:(1)碳酸钠溶液显碱性,能使酚酞试液变红色.
故填:红.
(2)反应I中,碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
故填:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)操作a的过程是蒸发浓缩、降温结晶、过滤.
故填:降温结晶.
(4)上述工艺流程中可循环利用的物质是二氧化碳.
故填:二氧化碳.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案
相关题目
4.下列实验现象的描述中,错误的是( )
| A. | 镁带在空气中燃烧,发出耀眼白光,放热,生成白色固体 | |
| B. | 把铁丝插入硫酸铜溶液中,铁丝表面会覆盖一层红色物质 | |
| C. | 硫在空气中燃烧产生淡蓝色火焰、放热、生成二氧化硫 | |
| D. | 木炭粉与氧化铜粉末混合高温加热,混合物中出现红色物质 |
19.密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下.下列说法正确的是( )
| 物 质 | A | B | C | D |
| 反应前质量/g | 19.7 | 8.7 | 31.6 | 0.4 |
| 反应后质量/g | 待测 | 17.4 | 0 | 3.6 |
| A. | 物质C一定是化合物,物质D一定是单质 | |
| B. | 反应后密闭容器中A的质量为19.7 g | |
| C. | 若物质A与物质C的相对分子质量之比为197:158,则反应中A与C的化学计量数之比为l:2 | |
| D. | 反应过程中,物质B与物质D变化的质量比为87:36 |
 如图所示是液态二氧化碳灭火器,请回答下列问题.
如图所示是液态二氧化碳灭火器,请回答下列问题.