题目内容
我们每时每刻都生活在空气的“海洋”里.科学家很早就开始了空气的研究.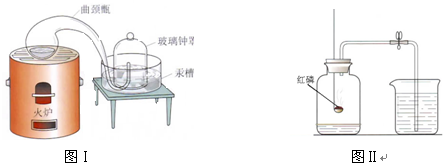
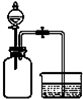
(1)200年前,拉瓦锡用图Ⅰ所示的装置研究了空气的组成.他把少量汞放在密闭的容器中连续加热,得到了红色的氧化汞粉末,同时钟罩内的汞液面上升.该化学反应的文字表达式或化学方程式是 .汞液面上升的原因是 .
(2)实验室中可用图Ⅱ所示的装置粗略研究空气的组成.红磷燃烧的主要现象为 ,反应的文字表达式或化学方程式是 .

(1)200年前,拉瓦锡用图Ⅰ所示的装置研究了空气的组成.他把少量汞放在密闭的容器中连续加热,得到了红色的氧化汞粉末,同时钟罩内的汞液面上升.该化学反应的文字表达式或化学方程式是
(2)实验室中可用图Ⅱ所示的装置粗略研究空气的组成.红磷燃烧的主要现象为
考点:空气组成的测定,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:(1)依据汞与氧气反应的产物写出反应的表达式结合氧气减小气压降低的分析问题;
(2)依据磷燃烧的产物及反应的现象分析回答.
(2)依据磷燃烧的产物及反应的现象分析回答.
解答:解:(1)汞与氧气加热反应时会生成氧化汞,从而消耗了氧气使钟罩内的压强变小导致汞的液面会上升;
(2)红磷的燃烧产物是五氧化二磷,明显的现象是剧烈燃烧,发出黄光,放出热量,生成大量的白烟;
故答案为:(1)汞+氧气
氧化汞(或2Hg+O2
2HgO);氧气与汞反应导致钟罩内气压降低;
(2)剧烈燃烧,发出黄光,放出大量的热,产生大量白烟;磷+氧气
五氧化二磷(或4P+5O2
2P2O5).
(2)红磷的燃烧产物是五氧化二磷,明显的现象是剧烈燃烧,发出黄光,放出热量,生成大量的白烟;
故答案为:(1)汞+氧气
| 加热 |
| ||
(2)剧烈燃烧,发出黄光,放出大量的热,产生大量白烟;磷+氧气
| 点燃 |
| ||
点评:此题是对有关空气中氧气含量测定的考查题,是基础性知识的考查题,只要认真分析,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目