题目内容
3.A、B、C、D为初中化学常见的化合物,它们由C、H、O、Na、Cl、Ca中的两种或三种元素组成,相对分子质量均小于100.(1)取少量A溶液,滴加紫色石蕊试剂,溶液呈蓝色,说明A的水溶液呈碱性,pH大于(填“大于”“小于”或“等于“)7.
(2)向上述溶液中通入少量的气体B,无明显现象,且反应后溶液仍呈蓝色.
(3)向(2)所得溶液中加入一定量C溶液,溶液变浑浊,过滤,滤液仍为蓝色.由此推断,A物质是NaOH(写化学式),产生浑浊的原因是Na2CO3+Ca(OH)2=2NaOH+CaCO3↓(填化学方程式表示).
(4)向(3)所得滤液中加入D溶液,有气泡产生,溶液变为红色,有关的化学方程式为2HCl+Na2CO3═2NaCl+H2O+CO2↑,NaOH+HCl=NaCl+H2O,最后所得溶液中的溶质是NaCl、HCl(指示剂除外).
分析 根据溶液A能使石蕊试液呈蓝色A的水溶液呈碱性,由H、C、O、Na、Cl、Ca中的两种或三种元素组成的物质中显碱性的物质有氢氧化钠、碳酸钠和氢氧化钙,碳酸钠的相对分子质量是106大于100,不符合题意,假设A是氢氧化钠,能与二氧化碳反应生成的碳酸钠溶液仍呈碱性,与氢氧化钙反应的生成了碳酸钙沉淀和氢氧化钠溶液,过滤后溶液仍呈碱性,碳酸钠与盐酸反应有气泡生成,则气体B为二氧化碳,C为氢氧化钙,D为盐酸,然后将推出的物质进行验证即可.
解答 解:由题意可知,由H、C、O、Na、Cl、Ca中的两种或三种元素组成的物质中显碱性的物质有氢氧化钠、碳酸钠和氢氧化钙,碳酸钠的相对分子质量是106大于100,不符合题意.假设A是氢氧化钠,能与二氧化碳反应生成的碳酸钠溶液仍呈碱性,与氢氧化钙反应的生成了碳酸钙沉淀和氢氧化钠溶液,过滤后的溶液仍呈碱性,碳酸钠能与盐酸反应有气泡生成,则气体B为二氧化碳,C为氢氧化钙,D为盐酸,带入题中验证,符合题意,属于
(1)A的水溶液呈碱性,pH大于7;
(3)通过推导可知,A物质是NaOH,产生浑浊现象的原因是:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(4)向滤液中加入盐酸溶液,有气泡产生,说明溶液中还有碳酸钠,溶液变为红色,说明加入的盐酸是过量的,有关的化学方程式为:2HCl+Na2CO3═2NaCl+H2O+CO2↑、NaOH+HCl=NaCl+H2O,最后得到的溶液中的溶质是:NaCl、HCl.
故答案为:(1)碱,大于;
(3)NaOH,Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(4)2HCl+Na2CO3═2NaCl+H2O+CO2↑、NaOH+HCl=NaCl+H2O,NaCl、HCl.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案| A. | 用过氧化氢和二氧化锰制取氧气 | |
| B. | 蒸发分离液态空气制得氮气和液氧 | |
| C. | 加热高锰酸钾制取氧气 | |
| D. | 加热氯酸钾和二氧化锰的混合物制取氧气 |
 物质之间常存在如图所示的“三角”关系,下列四组物质中均符合这一关系的是( )
物质之间常存在如图所示的“三角”关系,下列四组物质中均符合这一关系的是( )a.①H2O2 ②H2O ③O2
b.①Na2CO3 ②CO2 ③CaCO3
c.①CaCO3 ②CO2 ③Ca(OH)2
d.①C ②CO ③CO2.
| A. | abd | B. | abc | C. | bcd | D. | acd |
| A. | 胆矾研细 | B. | 石墨变金刚石 | C. | 灯泡发光 | D. | 冰雪融化 |
| A. | 工业上可以利用分离液态空气法制氧气 | |
| B. | 氧气可以支持燃烧,说明氧气具有可燃性 | |
| C. | 电解水时电源负极产生的气体可以燃烧,产生淡蓝色火焰 | |
| D. | 夏天鱼池内开启增氧泵,是因为温度升高,氧气在水中溶解量减少 |
| A. | 浓盐酸 | B. | 浓硫酸 | C. | 浓硝酸 | D. | 醋酸 |
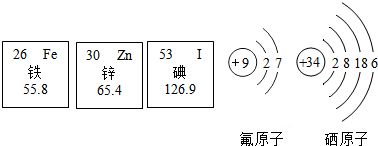
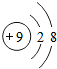 .
.
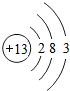 .
. 右图是实验室常用的两套气体发生装置
右图是实验室常用的两套气体发生装置