题目内容
20.某化学小组在AgNO3和Cu(NO3)2的混合溶液中加入一定质量的锌粉,充分反应后过滤,得到滤液和滤渣.他们对所得滤液和滤渣有如下描述:①滤液中一定含有Zn(NO3)2
②滤渣中一定含有Ag,可能含有Cu和Zn
③若滤液呈蓝色,则向滤液中滴加稀加稀盐酸会产生白色沉淀
④若向滤渣中滴加稀盐酸有气泡产生,则滤液中一定没有AgNO3和Cu(NO3)2.
上述四种描述中正确的个数为( )
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
分析 根据金属活动顺序表知:锌>铜>银,所以加入锌粉,首先锌粉和硝酸银溶液反应,置换出单质银,如果锌粉足量可以再继续和硝酸铜反应置换出铜.
解答 解::由题意可知金属活动性顺序可知,锌>铜>银.向含有AgNO3、Cu(NO3)2的混合液中加入一定量的锌粉,锌粉会首先置换硝酸银中的银,待硝酸银完全反应后继续与硝酸铜发生反应.
①滤液中一定含有Zn(NO3)2,正确;
②滤渣中一定含有Ag,可能含有Cu和Zn,正确;
③若滤液呈蓝色,则Cu(NO3)2未反应完或未反应,AgNO3可能完全反应也可能部分反应,故向滤渣中滴加稀盐酸不一定会产生白色沉淀,错误;
④若向滤渣中滴加稀盐酸有气泡产生,说明锌粉过量,AgNO3和Cu(NO3)2完全反应,则滤液中一定没有AgNO3和Cu(NO3)2.正确;
故选:C.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
10.现有下列试剂:硝酸银溶液、硫酸铝溶液、硫酸铜溶液、铝片、铜片.某小组设计了下列实验方案,请你和他们一起探究银、铝、铜三种金属的活动性强弱.
写出其中一个反应的化学方程式Cu+2AgNO3═Cu(NO3)2+2Ag等.
| 实验步骤 | 实验现象 | 结论 |
| 把铝片打磨后,放入硫酸铜溶液中,观察 | 铝片表面有红色物质析出 | 金属活动性由强到弱依次为: 铝、铜、银 |
| 把铜片打磨后,放入硝酸银溶液中,观察 | 铜片的表面有银白色物质析出 |
11.一种名为“污渍爆炸盐”的洗涤产品能高效去除衣物上的顽固污渍,是当前使用最为广泛的洗涤助剂之一.某校化学兴趣小组的同学在老师的指导下对该产品开展了以下探究活动.
【查阅资料】“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4,相对分子质量为122),它是一种白色粉末,易溶于水,且能与水反应,生成一种碳酸盐和一种强氧化性的物质.
【实验探究一】过碳酸钠的性质
为探究过碳酸钠的性质,同学们设计了以下实验,请按要求完成表格内容:
【实验探究二】过碳酸钠的含量测定
同学们经讨论设计了如图所示的实验装置.图中装置B盛装氢氧化钠溶液,C盛装澄清石灰水,D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气).
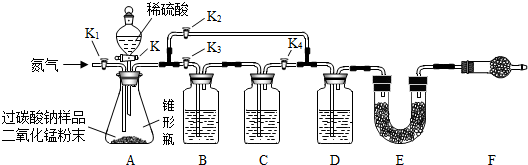
【实验讨论】
(1)①称量装置E的质量;②组装好装置,检查气密性,装入药品;③关闭活塞K,打开活塞K1,通入氮气;④关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气;⑤依次关闭活塞K1、K3、K4,打开活塞K K2、,直到反应不再进行;⑥再次称量装置E的质量.
以上实验步骤的正确顺序是D;
A.①②③④⑤⑥B.②①④⑤③⑥C.①②④⑤③⑥D.②④①⑤③⑥
(2)关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气排出装置中原有的空气,此时装置B的作用是除去原有空气中的二氧化碳,防止空气中的二氧化碳进入E装置;
(3)反应完全后关闭活塞K,打开活塞K1,通入氮气的目的是将装置中残留的二氧化碳排出,被E装置充分吸收;
(4)同学们称取6.63g含碳酸钠杂质的过碳酸钠样品(不含其他杂质)进行实验,根据实验后E装置增重2.42g,求该样品中过碳酸钠的含量(写出计算过程,结果保留小数点后一位).
(5)装置F的作用是防止空气中的二氧化碳和水蒸气进入E装置,干扰实验,若不连接装置F,测定的过碳酸钠含量会偏低(填“偏高”或“偏低”).
【查阅资料】“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4,相对分子质量为122),它是一种白色粉末,易溶于水,且能与水反应,生成一种碳酸盐和一种强氧化性的物质.
【实验探究一】过碳酸钠的性质
为探究过碳酸钠的性质,同学们设计了以下实验,请按要求完成表格内容:
| 序号 | 实验步骤 | 实验现象 | 实验分步结论(或解释) |
| ① | 向盛有过碳酸钠固体的试管中加入适量水 | 固体溶解 | 过碳酸钠易溶于水, 能与水发生反应. |
| ② | 向序号①的所得溶液中加入适量的二氧化锰粉末 | 有大量气泡 产生 | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ |
| ③ | 将带火星的木条置于试管口 | 木条复燃 | 序号②试管中产生的气体是; 过碳酸钠溶于水能生成过氧化氢. |
| ④ | 取序号③试管中的上层清液加入氯化钙溶液 | 产生白色 沉淀 | 反应的化学方程式Na2CO3+CaCl2═CaCO3↓+2NaCl. |
| 小结 | 过碳酸钠与水反应的化学方程式是Na2CO4+H2O═Na2CO3+H2O2. | ||
同学们经讨论设计了如图所示的实验装置.图中装置B盛装氢氧化钠溶液,C盛装澄清石灰水,D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气).

【实验讨论】
(1)①称量装置E的质量;②组装好装置,检查气密性,装入药品;③关闭活塞K,打开活塞K1,通入氮气;④关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气;⑤依次关闭活塞K1、K3、K4,打开活塞K K2、,直到反应不再进行;⑥再次称量装置E的质量.
以上实验步骤的正确顺序是D;
A.①②③④⑤⑥B.②①④⑤③⑥C.①②④⑤③⑥D.②④①⑤③⑥
(2)关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气排出装置中原有的空气,此时装置B的作用是除去原有空气中的二氧化碳,防止空气中的二氧化碳进入E装置;
(3)反应完全后关闭活塞K,打开活塞K1,通入氮气的目的是将装置中残留的二氧化碳排出,被E装置充分吸收;
(4)同学们称取6.63g含碳酸钠杂质的过碳酸钠样品(不含其他杂质)进行实验,根据实验后E装置增重2.42g,求该样品中过碳酸钠的含量(写出计算过程,结果保留小数点后一位).
(5)装置F的作用是防止空气中的二氧化碳和水蒸气进入E装置,干扰实验,若不连接装置F,测定的过碳酸钠含量会偏低(填“偏高”或“偏低”).
8.云南腾冲被称为翡翠之乡,翡翠中含有NaAlSi2O6,其中铝元素的是+3价,则NaAlSi2O6中Si的化合价为( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
15.下列选项分类不正确的是( )
| A. | 钢、黄铜、焊锡是合金 | B. | 蛋白质、维生素、油脂是供能物质 | ||
| C. | 甲烷、葡萄糖、尿素是有机物 | D. | Cu、I、Se都是人体必须的微量元素 |
5.清明时节,同学们相约外出踏青野炊.请用化学知识分析小丽问题:
(1)野炊食谱人表所示:
从合理膳食角度来看,你认为食谱中还应添加C(填字母);
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(2)野炊后同学们准备将垃圾分类处理,其中属于不可回收垃圾的是B(填字母);
A.废纸 B.果皮 C.易拉罐 D.塑料桶
(3)小滨用洗涤剂洗去手上的油迹,是利用了洗涤剂的乳化作用;
(4)大家在田边看到农民正在使用化肥NH4NO3,于是联想到NH4NO3不能和熟石灰混合施用,请用化学方程式解释原因2NH4NO3+Ca(OH)2=Ca(NO3)2+2NH3↑+2H2O.
(1)野炊食谱人表所示:
| 主食 | 馒头 |
| 配菜 | 红烧肉、豆腐汤、牛肉干 |
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(2)野炊后同学们准备将垃圾分类处理,其中属于不可回收垃圾的是B(填字母);
A.废纸 B.果皮 C.易拉罐 D.塑料桶
(3)小滨用洗涤剂洗去手上的油迹,是利用了洗涤剂的乳化作用;
(4)大家在田边看到农民正在使用化肥NH4NO3,于是联想到NH4NO3不能和熟石灰混合施用,请用化学方程式解释原因2NH4NO3+Ca(OH)2=Ca(NO3)2+2NH3↑+2H2O.
12.下列有关洗涤的说法中错误的是( )
| A. | 用热的氢氧化钠溶液洗手 | B. | 用洗洁精除去餐具上的油污 | ||
| C. | 用食醋洗去热水瓶中的水垢 | D. | 用稀盐酸洗去菜刀上的铁锈 |