题目内容
2.小敏同学学完实验室制取氧气后,分别进行了如下三次实验:(每次实验都反应完全)| 序号 | 所用试剂 | 产生氧气的质量(g) | 产生氧气的速率(g/s) |
| ① | ag氯酸钾固体 | W1 | V1 |
| ② | ag氯酸钾固体和bg二氧化锰固体 | W2 | V2 |
| ③ | ag氯酸钾固体和bg高锰酸钾固体 | W3 | V3 |
(2)V1=V2(填“<”、“=”、“>”)
(3)写出实验③中发生的化学反应符号表达式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
分析 根据ag氯酸钾固体加热产生氧气慢,ag氯酸钾固体和bg二氧化锰固体混合加热,产生氧气快,而催化剂在化学反应的前后质量不变,只是改变化学反应速率,不影响生成氧气的质量解答.根据实验室制取氧气的反应原理,直接加热高锰酸钾可制取氧气,而氯酸钾需加入二氧化锰做催化剂才能制取氧气解答.
解答 解:
(1)ag氯酸钾固体加热产生氧气慢,ag氯酸钾固体和bg二氧化锰固体混合加热,产生氧气快,高锰酸钾所起的作用主要有高锰酸钾分解产生的二氧化锰,可以作为氯酸钾制取氧气的催化剂,而催化剂在化学反应的前后质量不变,只是改变化学反应速率,不影响生成氧气的质量,故W1、W2、W3三者的关系是:W1=W2=W3;
(2)由反应原理可知:V1=V2;
(3)根据实验室制取氧气的反应原理,直接加热高锰酸钾可制取氧气,因此将氯酸钾和高锰酸钾的混合物加热制取氧气,先反应的物质名称是 高锰酸钾;反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;有二氧化锰产生后氯酸钾开始反应制取氧气,反应的化学方程式为:2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;在该实验中,高锰酸钾所起的作用主要有高锰酸钾分解产生的二氧化锰,可以作为氯酸钾制取氧气的催化剂.
答案:
(1)W1=W2=W3;
(2)=;
(3)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
点评 本题难度不大,了解制取氧气的方法、原理即可制取解答本题.考查实验室制取氧气的反应原理和书写化学方程式应注意:化学式、配平、反应条件、产物,是否存在箭头,才能顺利解题

| A. | 卟啉铁中含有5种元素 | B. | 卟啉铁中氢元素含量最低 | ||
| C. | 卟啉铁分子中含有34碳个原子 | D. | “缺铁性贫血”中的“铁”指单质铁 |
| A. | 钢铁生锈 | B. | 食物变馊 | C. | 动物呼吸 | D. | 鞭炮爆炸 |
| A. | 镁+氧气$\stackrel{点燃}{→}$氧化镁 | B. | 石蜡+氧气$\stackrel{点燃}{→}$水+二氧化碳 | ||
| C. | 氧化汞$\stackrel{加热}{→}$汞+氧气 | D. | 镁+盐酸→氢气+氯化镁 |
 小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强通过计算氮的质量分数发现该广告是虚假广告.
小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强通过计算氮的质量分数发现该广告是虚假广告.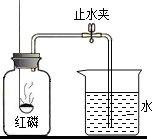 已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:
已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示: