题目内容
16.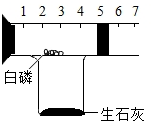 某同学设计了如图所示的装置来测定空气中氧气的含量.向烧杯内加水,引燃白磷,冷却至室温后,读取测量结果,观察到的实验现象是活塞先向右移,再向左移至4刻度处,请分析白磷燃烧的原因是:生石灰与水反应放热,使温度达到白磷的着火点,该反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
某同学设计了如图所示的装置来测定空气中氧气的含量.向烧杯内加水,引燃白磷,冷却至室温后,读取测量结果,观察到的实验现象是活塞先向右移,再向左移至4刻度处,请分析白磷燃烧的原因是:生石灰与水反应放热,使温度达到白磷的着火点,该反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
分析 根据生石灰与水反应放出大量的热,白磷在加热条件下,能和空气中的氧气发生反应,放出大量的热,据此进行分析解答.
解答 解:生石灰与水反应放出大量的热,使温度达到白磷的着火点,白磷燃烧,消耗了装置内的氧气,产生大量白烟,放出大量的热,装置内空气受热膨胀,活塞先向右移;由于氧气约占空气总体积的$\frac{1}{5}$,冷却至室温后,再向左移至4刻度处.
反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
故答案为:活塞先向右移,再向左移至4刻度处;生石灰与水反应放热,使温度达到白磷的着火点;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
点评 本题难度不大,掌握测定空气中氧气含量的实验原理、氧化钙的化学性质、燃烧的条件、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
相关题目
7.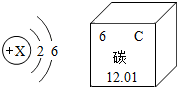 如图分别是R元素的原子结构示意图及碳元素在元素周期表中的相关信息,下列说法错误的是( )
如图分别是R元素的原子结构示意图及碳元素在元素周期表中的相关信息,下列说法错误的是( )
 如图分别是R元素的原子结构示意图及碳元素在元素周期表中的相关信息,下列说法错误的是( )
如图分别是R元素的原子结构示意图及碳元素在元素周期表中的相关信息,下列说法错误的是( )| A. | X=8 | |
| B. | 碳元素的相对原子质量为12.01 | |
| C. | 两种元素形成化合物的化学式可能是CR2 | |
| D. | R元素形成的离子符号是R4+ |
4.下列实验现象描述正确的是( )
| A. | 氢气在空气中燃烧产生淡蓝色火焰 | |
| B. | 红磷在空气中燃烧,产生白雾 | |
| C. | 铁在纯氧中剧烈燃烧、火星四射,生成四氧化三铁 | |
| D. | 木炭在氧气中完全燃烧,生成能使澄清石灰水变浑浊的二氧化碳气体 |
1.最近科学家发现,水在-157℃超低温、正常压力或真空集条件下仍呈液态,比蜂蜜还粘稠,下列关于这种“高密度液态水”的说法正确的是( )
| A. | 化学性质与普通水不同 | B. | 分子不再运动 | ||
| C. | 分子间的间隔比普通水大 | D. | 氢、氧两种原子的个数比为2:1 |
17.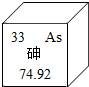 2014年3月24日,央视财经《经济半小时》曝光:湖南石门河砷超标1000多倍,需要长期进行砷污染土壤修复研究工作,在元素周期表中砷元素的某些信息如图所示,下列有关砷的说法错误的是( )
2014年3月24日,央视财经《经济半小时》曝光:湖南石门河砷超标1000多倍,需要长期进行砷污染土壤修复研究工作,在元素周期表中砷元素的某些信息如图所示,下列有关砷的说法错误的是( )
 2014年3月24日,央视财经《经济半小时》曝光:湖南石门河砷超标1000多倍,需要长期进行砷污染土壤修复研究工作,在元素周期表中砷元素的某些信息如图所示,下列有关砷的说法错误的是( )
2014年3月24日,央视财经《经济半小时》曝光:湖南石门河砷超标1000多倍,需要长期进行砷污染土壤修复研究工作,在元素周期表中砷元素的某些信息如图所示,下列有关砷的说法错误的是( )| A. | 砷是一种高毒性的非金属元素 | |
| B. | 砷元素的原子核内质子数为33 | |
| C. | 砷元素的相对原子质量为74.92 | |
| D. | 砒霜的主要成分为三氧化二砷,其中砷元素化合价为-3 |
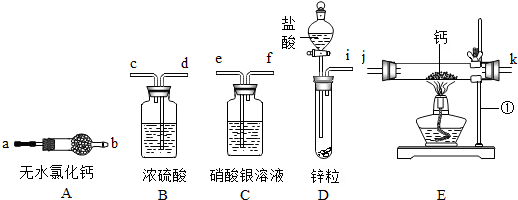
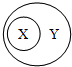 下列选项符合图示包含关系的是( )
下列选项符合图示包含关系的是( )