题目内容
科学家采取“组合转化”技术,使CO2和H2发生反应,生成一种化工原化学方程式为:2CO2+6H2═乙烯+4H2O,则乙烯的化学式为 .
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:根据质量守恒定律:反应前后原子的种类和数目不变分析乙烯的化学式.
解答:解:
在反应2CO2+6H2═乙烯+4H2O中:
反应物中原子个数…生成物中原子个数
碳:2…未知
氢:12…8
氧:4…4
由质量守恒定律化学反应前后原子的种类和数目都不变,反应生成的乙烯中含有两个碳原子和四个氢原子,其化学式为C2H4.
故答案为:C2H4.
在反应2CO2+6H2═乙烯+4H2O中:
反应物中原子个数…生成物中原子个数
碳:2…未知
氢:12…8
氧:4…4
由质量守恒定律化学反应前后原子的种类和数目都不变,反应生成的乙烯中含有两个碳原子和四个氢原子,其化学式为C2H4.
故答案为:C2H4.
点评:本题主要考查了质量守恒定律应用,难度不大,属于基础性的知识,应加强基础知识的学习.

练习册系列答案
相关题目
某研究小组测定Cu-Fe合金和Fe-Al合金中铁的质量分数.向5.6g其中一种合金粉末中加入100g某溶质质量分数的稀硫酸,恰好完全反应,并产生Xg氢气,则下列说法不正确的( )
| A、当粉末为Fe-Al合金时,X一定不等于0.2g |
| B、当粉末为Cu一Fe合金时,若X为0.1g,则该种合金中含铜的质量分数为50% |
| C、当粉末为Fe-Al合金时,所需稀硫酸溶质质量分数可能等于9.8% |
| D、当粉末为Cu一Fe合金时,反应完全后溶液里的溶质只有一种 |
用水壶烧开水,水沸腾后壶盖被顶起,说明( )
| A、分子间空隙增大 |
| B、分子的质量很小 |
| C、分子的体积变大 |
| D、分子是由原子构成的 |
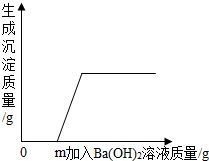 某溶液由氯化钾溶液、稀硝酸、稀硫酸和硝酸铜溶液中的一种或几种混合而成.取一定量该溶液,向其中滴加Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液质量的关系如图所示,则下列关于溶液中溶质的判断正确的是( )
某溶液由氯化钾溶液、稀硝酸、稀硫酸和硝酸铜溶液中的一种或几种混合而成.取一定量该溶液,向其中滴加Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液质量的关系如图所示,则下列关于溶液中溶质的判断正确的是( )| A、肯定没有氯化钾 |
| B、肯定有硫酸 |
| C、是否含有硝酸铜不能确定 |
| D、肯定含有硝酸 |
加油站必须粘贴的标志是( )
A、 |
B、 |
C、 |
D、 |
 用所学的化学知识解答下列问题.
用所学的化学知识解答下列问题. 最近网络上流行着一个有趣的实验“大象的牙膏”:在细长的容器中加入双氧水和发泡剂(用于产生泡沫),仅看到少量泡沫,然后向其中加入少量物质M,立即看到大量泡沫迅速从瓶口喷出,源源不断就像挤不完的牙膏.
最近网络上流行着一个有趣的实验“大象的牙膏”:在细长的容器中加入双氧水和发泡剂(用于产生泡沫),仅看到少量泡沫,然后向其中加入少量物质M,立即看到大量泡沫迅速从瓶口喷出,源源不断就像挤不完的牙膏.