题目内容
13.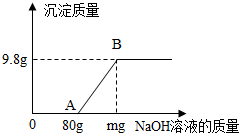 杯中装有一定量硫酸和硫酸铜的混合溶液,某同学向烧杯中逐渐加入10%的NaOH溶液,将得到沉淀的质量(纵坐标)与所加入NaOH溶液的质量(横坐标)关系以图象的形式记录如图:
杯中装有一定量硫酸和硫酸铜的混合溶液,某同学向烧杯中逐渐加入10%的NaOH溶液,将得到沉淀的质量(纵坐标)与所加入NaOH溶液的质量(横坐标)关系以图象的形式记录如图:(1)OA一段没有沉淀产生的原因是2NaOH+H2SO4═Na2SO4+2H2O(用化学方程式表示).
(2)请计算m的值(写出计算过程).
分析 稀硫酸先和氢氧化钠反应生成硫酸钠和水,当稀硫酸完全反应后,硫酸铜再和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠;
根据提供的数据可以计算m的值.
解答 解:(1)OA一段没有沉淀产生的原因是稀硫酸和氢氧化钠反应生成硫酸钠和水,反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O;
故填:2NaOH+H2SO4═Na2SO4+2H2O.
(2)解:设与CuSO4反应的NaOH的质量为x,
CuSO4+2NaOH═Cu(OH)2↓+Na2SO4,
80 98
x 9.8g
$\frac{80}{x}$$\frac{98}{9.8g}$,
x=8g,
与CuSO4反应的NaOH溶液的质量为:8g÷10%=80g,
参加反应的NaOH溶液的总质量为:80g+80g=160g,
答:m的值为160.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目
4.分类是学习和研究化学的常用方法.下列分类正确的是( )
| A. | 蒸馏水和矿泉水:硬水 | B. | 金刚石和石墨:碳单质 | ||
| C. | 生铁和玻璃钢:金属材料 | D. | 氧化钾和碳酸氢铵:盐类 |
1.2015年两会期间,环境问题成了热议的话题之一.近几年来,雾霾在我国多地频发,雾霾可导致呼吸系统疾病人增多,因为雾霾可使空气中增加大量的( )
| A. | 二氧化碳 | B. | 一氧化碳 | C. | 二氧化碳 | D. | 可吸入颗粒物 |
5.下列说法正确的是( )
| A. | 向稀硫酸中滴入几滴NaOH溶液,再滴加CuSO4溶液,不一定有蓝色沉淀生成 | |
| B. | 鸡蛋清中加入饱和硫酸铵溶液,蛋白质会变性 | |
| C. | 溶液中析出晶体时,溶质减少,则溶质的质量分数一定减小 | |
| D. | 某化肥中加熟石灰研磨,未闻到氨臭味,该化肥一定不是氮肥 |
3.现有12gA和足量的B混合加热,A与B发生化学反应,12gA完全反应后生成8gC和6gD,则参加反应的A与B的质量比是( )
| A. | 4:1 | B. | 5:1 | C. | 6:1 | D. | 7:1 |


 向一定量的饱和Ca(OH)2溶液中加入一定量的生石灰
向一定量的饱和Ca(OH)2溶液中加入一定量的生石灰 相同质量的Mg、Fe分别与稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V
相同质量的Mg、Fe分别与稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V 向一定量的KOH和Ba(NO3)2的混合溶液中,逐滴加入稀H2SO4
向一定量的KOH和Ba(NO3)2的混合溶液中,逐滴加入稀H2SO4 向一定量的HCl和CaCl2(CaCl2溶液呈中性)的混合液中加入Na2CO3溶液.
向一定量的HCl和CaCl2(CaCl2溶液呈中性)的混合液中加入Na2CO3溶液.