题目内容
图中是A、B、C三种固体物质的溶解度曲线图.
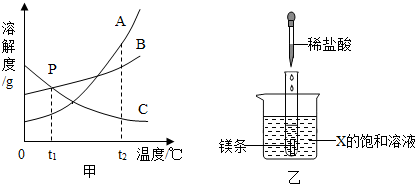
(1)甲图中,t2℃时,A、B、C三种物质中溶解度最大的是 .P点所表示的含义为 .
(2)t℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法有 (答一条即可).
(3)如图乙所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入10mL稀盐酸,立即产生大量的气泡,该反应的化学方程式为 ,反应中会 (填“吸热”或“放热”).同时烧杯中会出现浑浊,则X可能为A、B、C三种物质中的哪一种? .

(1)甲图中,t2℃时,A、B、C三种物质中溶解度最大的是
(2)t℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法有
(3)如图乙所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入10mL稀盐酸,立即产生大量的气泡,该反应的化学方程式为
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,物质发生化学变化时的能量变化,书写化学方程式、文字表达式、电离方程式
专题:溶液、浊液与溶解度
分析:(1)根据固体物质的溶解度曲线可知:①不同物质在同一温度下的溶解度的大小,②溶解度曲线的交点表示该温度下两物质的溶解度相等;
(2)使饱和溶液变为不饱和溶液,可采取升温、蒸发溶剂、加入溶质的方法;
(3)镁和盐酸反应生成氯化镁和氢气,据此书写方程式,该反应放热,烧杯中出现浑浊,说明该物质的溶解度随温度的升高而减小.
(2)使饱和溶液变为不饱和溶液,可采取升温、蒸发溶剂、加入溶质的方法;
(3)镁和盐酸反应生成氯化镁和氢气,据此书写方程式,该反应放热,烧杯中出现浑浊,说明该物质的溶解度随温度的升高而减小.
解答:解:(1)观察三种物质的溶解度曲线不难看出,t2℃时三种物质的溶解度最大的是A,P点是B和C的溶解度曲线的交点,即在该温度下,两种物质的溶解度相等;(2)由于B的溶解度随温度的升高而增大,因此将物质的不饱和溶液转变成饱和溶液可采取的方法是降温、增加溶质或蒸发溶剂,但温度不变,故可采取加入溶质、恒温蒸发溶剂的方法;
(3)镁和盐酸反应生成氯化镁和氢气,反应方程式是Mg+2HCl═MgCl2+H2↑;由于镁条和稀盐酸反应是放热反应,烧杯内出现浑浊,说明X的溶解度随温度的升高而减小,而C的溶解度随温度的升高而减小;
故答案为:(1)A;t1℃时BC的溶解度相等;
(2)加入B(或恒温蒸发溶剂);
(3)Mg+2HCl═MgCl2+H2↑;C.
(3)镁和盐酸反应生成氯化镁和氢气,反应方程式是Mg+2HCl═MgCl2+H2↑;由于镁条和稀盐酸反应是放热反应,烧杯内出现浑浊,说明X的溶解度随温度的升高而减小,而C的溶解度随温度的升高而减小;
故答案为:(1)A;t1℃时BC的溶解度相等;
(2)加入B(或恒温蒸发溶剂);
(3)Mg+2HCl═MgCl2+H2↑;C.
点评:本题主要考查了固体溶解度曲线的意义及根据溶解度曲线解决相关的问题,培养学生分析问题、解决问题的能力.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
海底不仅蕴藏着大量的煤、石油、天然气等常规化石燃料,人们还在海底发现了一种新型矿石资源--天然气水合物,它的主要成分是( )
| A、冰 | B、干冰 | C、甲烷 | D、煤和石油 |
密闭在针管中的液态水变成气态的水的变化过程中水分子发生了什么变化( )
| A、水分子本身变大 |
| B、水分子之间间隔变大 |
| C、水分子数目增多 |
| D、水分子受热到针管另一端 |
火箭主要燃料是偏二甲肼(化学式为C2H8N2).下列有关偏二甲肼的叙述正确的是( )
| A、偏二甲肼是由2个碳原子、4个氢原子、1个氮气分子组成 |
| B、偏二甲肼是由碳、氢、氮三种元素组成 |
| C、偏二甲肼是由2个碳原子、8个氢原子、2个氮气分子组成 |
| D、偏二甲肼中碳、氢、氮 的质量1:4:1 |
 在一公共场所看见一则如图所示广告.
在一公共场所看见一则如图所示广告.