题目内容
7.已知一个碳12原子的质量为1.993×10-26kg,一个镁原子的质量为4.037×10-26kg,(1)根据数据比较:相同质量的碳、镁两种物质所含原子个数较多的是碳原子;
(2)试分别列式计算碳原子、镁原子的相对原子质量.(结果保留整数)
(3)分别含6.02×1023个原子的碳、镁两种物质,质量比是1:2.(结果保留整数)
分析 根据已有的相对原子质量的概念以及公式进行分析解答即可.
解答 解:(1)一个碳原子的质量小于一个镁原子的质量,故相同质量的碳、镁两种物质所含原子个数较多的是碳原子,故填:碳原子;
(2)镁原子的相对原子质量$\frac{4.037×1{0}^{-26}kg}{1.993×1{0}^{-26}kg×\frac{1}{12}}$=24
碳原子的相对原子质量:$\frac{1.993×1{0}^{-26}kg}{1.993×1{0}^{-26}kg×\frac{1}{12}}$=12
故答案为:24,12;
(3)含有相同原子的碳、镁两种物质的质量比就是这两种原子的相对原子质量之比,即12:24=1:2,故填:1:2.
点评 本题考查的是有关相对原子质量的计算的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
15.下列气体中,能供给动植物呼吸的是( )
| A. | 氢气 | B. | 氧气 | C. | 二氧化硫 | D. | 二氧化碳 |
17.若6g某物质在空气中完全燃烧生成8.8g二氧化碳和3.6g水(只有这两种产物),则关于这种物质的描述正确的是( )
| A. | 该物质由碳、氢两种元素组成 | |
| B. | 该物质由碳、氢、氧三种元素组成 | |
| C. | 该物质中碳元素与氢元素的质量比为4:1 | |
| D. | 该物质的分子中碳原子与氢原子的个数比为1:3 |
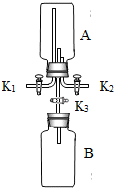 某研究性学习小组尝试利用氨气进行“微粒的基本性质”的实验探究,实验过程如下:
某研究性学习小组尝试利用氨气进行“微粒的基本性质”的实验探究,实验过程如下: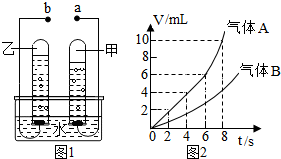 如图分别是电解水的简易装置图和电解水生成气体的体积与时间的关系图,下列分析正确的是C.
如图分别是电解水的简易装置图和电解水生成气体的体积与时间的关系图,下列分析正确的是C.