题目内容
15.某工厂综合加工海水的主要步骤如图所示,请根据图示回答下列问题: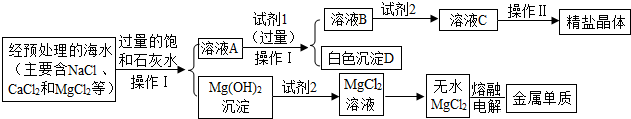
(1)操作I的名称是过滤.此操作用到的玻璃仪器有烧杯、玻璃棒、漏斗.此步反应的化学方程式MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓.
(2)试剂1是Na2CO3(写化学式,下同),白色沉淀D是CaCO3.
(3)溶液B中含有的溶质是NaCl、NaOH、Na2CO3.向溶液B加入试剂2的作用除去溶液B中NaOH和Na2CO3,加入试剂2后,在溶液中可观察到有气泡产生的现象.
(4)写出Mg(OH)2沉淀与试剂2反应的化学方程式Mg(OH)2+2HCl=MgCl2+2H2O.
(5)在熔融状态下电解无水氯化镁会产生一种金属单质和一种双原子分子的气体单质,该反应的化学方程式是MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
分析 过滤可以把沉淀和溶液分离;碳酸钠能和氯化钙、氢氧化钙等物质反应;稀盐酸能和碳酸钠、氢氧化钠等物质反应;电解氯化镁能生成镁和氯气.
解答 解:(1)向海水中加入石灰水后,氢氧化钙能和氯化镁反应生成氢氧化镁沉淀,通过过滤可以把沉淀和溶液分离.用到的玻璃仪器还有漏斗;氢氧化钙与氯化镁反应生成氯化钙和氢氧化镁白色沉淀;
故填:过滤;漏斗;MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓
(2)溶液A中含有氯化钠、氯化钙、氢氧化钙等物质,加入碳酸钠溶液可以把氯化钙、氢氧化钙转化为碳酸钙沉淀、氯化钠和氢氧化钠.
故填:Na2CO3;CaCO3.
(3)溶液B中含有的溶质有:氯化钠、氢氧化钠、碳酸钠.试剂2是稀盐酸,向溶液B加入稀盐酸后,稀盐酸能和碳酸钠反应生成二氧化碳,所以在溶液中可观察到有气泡产生.
故填:NaCl、NaOH、Na2CO3;除去溶液B中NaOH和Na2CO3;有气泡产生
(4)氢氧化镁与稀盐酸反应生成氯化镁和水,故填:Mg(OH)2+2HCl=MgCl2+2H2O
(5)电解氯化镁的化学方程式为:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
故填:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑
点评 本题主要考查实验操作、物质之间相互作用、化学方程式的书写等方面的知识,书写化学方程式要注意规范性.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
3.下列实验现象的描述正确的是( )
| A. | 蜡烛在空气中燃烧生成二氧化碳和水 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰 | |
| C. | 红磷在空气中燃烧产生大量白色烟雾 | |
| D. | 铁丝在氧气中燃烧,火星四射,生成黑色固体,放出大量的热 |
10.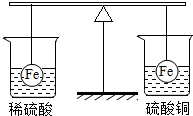 如图所示,在等臂杠杆的两端各系一只等质量等体积的铁球,这时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,下列说法正确的是( )
如图所示,在等臂杠杆的两端各系一只等质量等体积的铁球,这时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,下列说法正确的是( )
 如图所示,在等臂杠杆的两端各系一只等质量等体积的铁球,这时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,下列说法正确的是( )
如图所示,在等臂杠杆的两端各系一只等质量等体积的铁球,这时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,下列说法正确的是( )| A. | 左边烧杯中溶液质量减少 | B. | 右边烧杯中溶液的质量增加 | ||
| C. | 杠杆仍保持平衡 | D. | 杠杆向右倾斜 |
20.苯甲酸[C6H5COOH]是一种弱酸,具有酸的性质,可做食品防腐剂.下列关于苯甲酸说法不正确的是( )
| A. | 它是由3种元素组成的 | |
| B. | 苯甲酸可与NaOH发生中和反应 | |
| C. | 苯甲酸中碳元素与氧元素的质量比21:8 | |
| D. | 苯甲酸由7个碳原子、6个氢原子、2个氧原子构成 |
5.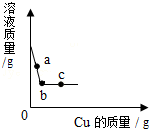 向一定质量的AgNO3溶液中加入Cu,溶液质量与加入Cu的质量关系如图所示,下列说法中不正确的是( )
向一定质量的AgNO3溶液中加入Cu,溶液质量与加入Cu的质量关系如图所示,下列说法中不正确的是( )
 向一定质量的AgNO3溶液中加入Cu,溶液质量与加入Cu的质量关系如图所示,下列说法中不正确的是( )
向一定质量的AgNO3溶液中加入Cu,溶液质量与加入Cu的质量关系如图所示,下列说法中不正确的是( )| A. | a点对应溶液中的溶质有2种 | B. | b点对应固体只有Ag | ||
| C. | b~c段对应溶液中含有AgNO3 | D. | c点时反应已经停止 |