题目内容
将铁合金置于氧气中燃烧,得到0.44g二氧化碳和29g四氧化三铁,则铁合金是
A.纯铁 B.钢 C.生铁 D.无法计算
B
【解析】
试题分析: 二氧化碳的化学式为CO2,生成0.44g的二氧化碳中,碳元素的质量为0.44g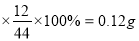 ,四氧化三铁的化学式为Fe3O4,生成29g四氧化三铁中,铁元素的质量为29g
,四氧化三铁的化学式为Fe3O4,生成29g四氧化三铁中,铁元素的质量为29g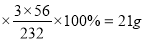 ,根据质量守恒定律,生成物中含有碳元素和铁元素的总质量是0.12g +21g=21.12g,则反应前铁合金的质量也是21.12g,则碳元素的质量分数为
,根据质量守恒定律,生成物中含有碳元素和铁元素的总质量是0.12g +21g=21.12g,则反应前铁合金的质量也是21.12g,则碳元素的质量分数为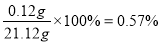 ,钢的含碳量为0.03%—2%,所以,该铁合金为钢。
,钢的含碳量为0.03%—2%,所以,该铁合金为钢。
考点:质量守恒定律的应用

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 3Fe+4CO2
3Fe+4CO2

