题目内容
9.将下列化学式中的原子团标出化合价CuSO4 NaNO3 CaCO3 NH4Cl Mg(OH)2.
分析 硫酸铜中的原子团是硫酸根,化合价是-2;
硝酸钠中的原子团是硝酸根,化合价是-1;
碳酸钙中的原子团是碳酸根,化合价是-2;
氯化铵中的原子团是铵根,化合价是+1;
氢氧化镁中的原子团是氢氧根,化合价是-1.
解答 解:硫酸铜、硝酸钠、碳酸钙、氯化铵和氢氧化镁中的原子团及其化合价如下所示:
Cu$\stackrel{-2}{{SO}_{4}}$、Na$\stackrel{-1}{{NO}_{3}}$、Ca$\stackrel{-2}{{CO}_{3}}$、$\stackrel{+1}{{NH}_{4}}$Cl、Mg$\stackrel{-1}{{(OH)}_{2}}$.
故答案为:Cu$\stackrel{-2}{{SO}_{4}}$、Na$\stackrel{-1}{{NO}_{3}}$、Ca$\stackrel{-2}{{CO}_{3}}$、$\stackrel{+1}{{NH}_{4}}$Cl、Mg$\stackrel{-1}{{(OH)}_{2}}$.
点评 元素或原子团的化合价应该标在元素符号或原子团的正上方,要注意理解.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
10.下列几种说法,其中正确的( )
| A. | 盐水的沸点比水低 | |
| B. | 汽油洗去油污的原理是乳化 | |
| C. | 蒸发食盐水时,要用玻璃棒不断搅拌,用酒精灯持续加热,直到蒸干为止 | |
| D. | 气体的溶解度一般随温度的升高而减小 |
7.图中能正确反映题中所描述的变化事实的是( )
| A. | 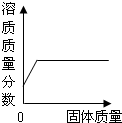 接近饱和的氯化钠溶液中加入氯化钠固体 | |
| B. |  不饱和硝酸钾溶液升温 | |
| C. |  一定量水中加入硝酸钾固体 | |
| D. |  加热蒸发不饱和的氯化钠溶液 |
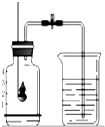 如图是空气中氧气含量的测定装置.试回答:
如图是空气中氧气含量的测定装置.试回答: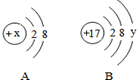 如图中A、B分别是某微粒的结构示意图,回答下列问题:
如图中A、B分别是某微粒的结构示意图,回答下列问题: