题目内容
水在生活、生产和化学实验中起着十分重要的作用.
(1)某自来水厂生产的主要步骤为:河水→A(明矾)→B(沉淀)→C(过滤)→D(加液氯)→净水.这一过程中加明矾的[化学式为KAl(SO4)2?12H2O]作用是 ,明矾中含有的原子团名称为 ;加液氯的目的是 .
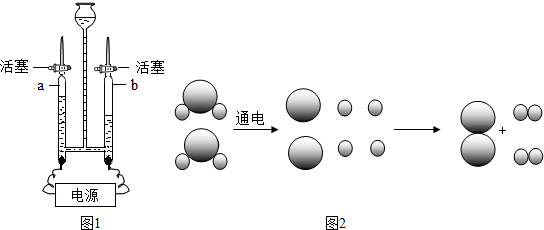
(2)电解水实验如图1所示,a玻璃管中生成的气体是 ,检验该气体的方法是 .电解水发生化学反应的示意图如图2:
从示意图中可获得的正确信息是 (填写编号).
A.反应前后共有6种原子,4种分子
B.反应前后元素种类不变,都为3种
C.化学变化的实质是原子的重新组合
D.化学变化中分子是最小的微粒
E.该化学反应中,氢、氧两种分子的个数比是2:1
F.水是由氢气和氧气组成
电解水的化学方程式为 .

(1)某自来水厂生产的主要步骤为:河水→A(明矾)→B(沉淀)→C(过滤)→D(加液氯)→净水.这一过程中加明矾的[化学式为KAl(SO4)2?12H2O]作用是
(2)电解水实验如图1所示,a玻璃管中生成的气体是
从示意图中可获得的正确信息是
A.反应前后共有6种原子,4种分子
B.反应前后元素种类不变,都为3种
C.化学变化的实质是原子的重新组合
D.化学变化中分子是最小的微粒
E.该化学反应中,氢、氧两种分子的个数比是2:1
F.水是由氢气和氧气组成
电解水的化学方程式为
考点:自来水的生产过程与净化方法,电解水实验,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:(1)根据明矾是净水剂,能除去水中的悬浮物、明矾中含有的原子团为硫酸根以及加液氯的目的是消毒杀菌进行解答;
(2)根据电解水生成氢气和氧气,其中氢气和氧气的体积比为2:1进行解答.
(2)根据电解水生成氢气和氧气,其中氢气和氧气的体积比为2:1进行解答.
解答:解:(1)明矾是净水剂,能除去水中的悬浮物,明矾中含有的原子团为硫酸根,加液氯的目的是消毒杀菌;
(2)电解水生成氢气和氧气,其中氢气和氧气的体积比为2:1,所以a玻璃管中生成的气体是氧气,检验该气体的方法带火星的木条,观察是否复燃.从示意图中可获得的正确信息是化学变化的实质是原子的重新组合、该化学反应中,氢、氧两种分子的个数比是2:1,反应前后共有2种原子,3种分子;反应前后元素种类不变,都为2种;化学变化中原子是最小的微粒;水是由氢元素和氧元素组成,电解水的化学方程式为2H2O
2H2↑+O2↑.
故答案为:(1)除去悬浮物;硫酸根;消毒杀菌;
(2)氧气;带火星的木条,观察是否复燃;CE;2H2O
2H2↑+O2↑.
(2)电解水生成氢气和氧气,其中氢气和氧气的体积比为2:1,所以a玻璃管中生成的气体是氧气,检验该气体的方法带火星的木条,观察是否复燃.从示意图中可获得的正确信息是化学变化的实质是原子的重新组合、该化学反应中,氢、氧两种分子的个数比是2:1,反应前后共有2种原子,3种分子;反应前后元素种类不变,都为2种;化学变化中原子是最小的微粒;水是由氢元素和氧元素组成,电解水的化学方程式为2H2O
| ||
故答案为:(1)除去悬浮物;硫酸根;消毒杀菌;
(2)氧气;带火星的木条,观察是否复燃;CE;2H2O
| ||
点评:本题主要考查了水的组成、净化的知识,难度不大,但涉及的知识点较多.加强基础知识的学习,是解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质中,含有氧分子的是( )
| A、O2 |
| B、H2O2 |
| C、SO2 |
| D、NO2 |
某无色气体可能含有H2、CO、CH4中的一种或几种,依次进行下列实验(假设每步反应或吸收均完全):①无色气体在足量的氧气中充分燃烧;②将生成的气体通过盛有浓硫酸的洗气瓶吸收气体中的水蒸气,装置质量增加10.8g;③再将剩余气体通过盛有足量Ca(OH)2溶液的洗气瓶,装置质量增加13.2g.下列推断正确的是( )
| A、该气体可能有H2和CH4组成 |
| B、该气体可能由CO和CH4组成 |
| C、该气体可能只含有CH4 |
| D、该气体的组成有五种可能 |
下列化学方程式所表示的化学反应能发生的是( )
| A、Cu+H2SO4═CuSO4+H2↑ |
| B、Fe+Zn( NO3)2═Fe(NO3)2+Zn↓ |
| C、CuCl2+2NaOH═Cu(OH)2↓+2NaCl |
| D、Na2CO3+2KNO3═K2CO3+2NaNO3 |
不会造成空气污染的物质是( )
| A、PM2.5 | B、一氧化碳 |
| C、氮气 | D、二氧化硫 |
 可知,氮原子最外层电子数目为
可知,氮原子最外层电子数目为