题目内容
1.下列变化是化学变化的是( )| A. | 汽油挥发 | B. | 车胎放炮 | C. | 灯泡发光 | D. | 粮食酿酒 |
分析 化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
解答 解:A、汽油挥发过程中没有新物质生成,属于物理变化.
B、车胎放炮是由于气体压强大造成的,没有新物质生成,属于物理变化.
C、灯泡发光的过程中没有新物质生成,属于物理变化.
D、粮食酿成酒过程中有新物质酒精生成,属于化学变化.
故选:D.
点评 本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.

练习册系列答案
相关题目
11.在一次化学实验中,同学们将饱和CuSO4溶液逐滴加到5ml饱和NaOH溶液中,观察到以下异常实验现象:
(1)在实验①中同学们根据所学初中化学知识判断蓝色沉淀是Cu(OH)2,请你写出生成蓝色沉淀的化学方程式CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(2)已知:Ⅰ.Cu(OH)2在室温下稳定,70℃~80℃时可脱水分解生成CuO;Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色:
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究:小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解,其他同学一致否定了他的猜测,理由是沉淀消失,形成亮蓝色溶液,而氢氧化铜分解产生的是黑色固体(合理即可);
(3)同学们交流讨论后,提出以下两种猜想:猜想一:少许Cu(OH)2可溶于足量水中;猜想二:Cu(OH)2粉末(其它试剂可任选)设计如下实验,请你填写表中的空格:
(4)根据实验,并进一步查阅资料知道,Cu(OH)2在浓NaOH溶液中溶解生成Na2Cu(OH)4,反应的化学方程式是Cu(OH)2+2NaOH=Na2Cu(OH)4;根据实验可知饱和CuSO4溶液与饱和NaOH溶液的反应是放热反应,依据的实验现象是资料Ⅰ显示Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO,而表格1可知随着氢氧化钠溶液的滴加,观察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色(合理即可).
| 实验序号 | 滴加CuSO4 | 实验现象 |
| ① | 第1-6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7-9滴 | 产生蓝色沉淀,且沉淀逐渐增多,振荡后沉淀不消失,很快沉淀逐渐变黑色 |
(2)已知:Ⅰ.Cu(OH)2在室温下稳定,70℃~80℃时可脱水分解生成CuO;Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色:
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究:小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解,其他同学一致否定了他的猜测,理由是沉淀消失,形成亮蓝色溶液,而氢氧化铜分解产生的是黑色固体(合理即可);
(3)同学们交流讨论后,提出以下两种猜想:猜想一:少许Cu(OH)2可溶于足量水中;猜想二:Cu(OH)2粉末(其它试剂可任选)设计如下实验,请你填写表中的空格:
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5ml蒸馏水中,充分振荡 | 沉淀不消失 | 猜想一错误 |
| ④ | 将少许Cu(OH)2粉末加到NaOH浓溶液中,充分振荡 | 沉淀消失,溶液变成亮蓝色 | 猜想二正确 |
12.下列有关溶液的叙述,正确的是( )
| A. | 均一、稳定的液体都是溶液 | |
| B. | 溶液稀释前后,溶质的质量不变 | |
| C. | 固体物质的溶解度都随温度的升高而增大 | |
| D. | 饱和溶液一定是浓溶液 |
9.下列物质的变化,其中一种与其它三种有本质差别的是( )
| A. | 打开盛有浓盐酸的试剂瓶,从瓶口涌出大量白雾 | |
| B. | 光亮的铝片放置在空气中,表面变暗 | |
| C. | 石油分馏后得到汽油、煤油和柴油 | |
| D. | 干冰升华变成气体物质 |
6.下列实验操作错误的是( )
| A. | 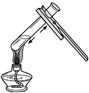 加热液体 | B. | 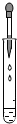 滴加液体 | C. | 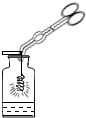 铁丝在O2中燃烧 | D. | 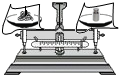 称量氯化钠 |
13.下列关于自然界中水的说法不正确的是( )
| A. | 将井水煮沸腾既能使其硬度降低,又能消毒 | |
| B. | 软水是指不含Ca2+、Mg2+的水 | |
| C. | 可用肥皂水区别硬水和软水 | |
| D. | 我省人均淡水资源量匮乏 |
10.一个密闭容器中,在点燃的条件下C2H2与O2恰好完全反应,测得部分数据如表:
下列说法不正确的是( )
| 物质 | C2H2 | O2 | CO2 | X | H2O |
| 反应前质量/g | 2.6 | 7.2 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 6.6 | 待测 | 1.8 |
| A. | 待测物的质量为1.4g | B. | X物质为CO | ||
| C. | 该化学反应为氧化反应 | D. | CO2与X的化学计量数之比为1:3 |
11.现取氯化钙和碳酸钙混合物样品进行实验,将150mL的稀盐酸分三次加入装有15g样品的烧杯中,每次充分反应后测得生成气体的质量,实验数据如下表(不考虑实验消耗).
试求:
(1)m的值时2g.
(2)实验后所得溶液中溶质氯化钙的质量(保留一位小数).
| 实验 | 第一次 | 第二次 | 第三次 |
| 加入稀盐酸的量/ml | 50 | 50 | 50 |
| 生成气体的质量/g | 2 | m | 0.4 |
(1)m的值时2g.
(2)实验后所得溶液中溶质氯化钙的质量(保留一位小数).