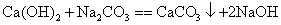题目内容
Na2CO3与盐酸反应分两步进行:
第一步反应为:Na2CO3+HCl===NaCl+NaHCO3;
第二步反应为:NaHCO3+HCl===NaCl+H2O+CO2↑
 取Na2CO3溶液100g,逐滴加入稀盐酸直到过量。反应过程中产生的气体质量与加入
取Na2CO3溶液100g,逐滴加入稀盐酸直到过量。反应过程中产生的气体质量与加入
的盐酸质量的关系如图所示:
 (1)反应中最多可以产生CO2___________g。
(1)反应中最多可以产生CO2___________g。
(2)求Na2CO3溶液中溶质质量分数(要求书写计算过程)。
(相对原子质量:C—12、Na—23、H—1、O—16)
(1)4.4(2分)
(2)解法一:设第②步反应中参加反应的NaHCO3的质量为x
NaHCO3+HCl===NaCl+H2O+CO2↑
84 44
x 4.4 g

 x=8.4 g
x=8.4 g
设参加反应的Na2CO3的质量为y
Na2CO3+HCl===NaHCO3+NaCl
106 84
y 8.4 g

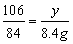 y=10.6 g
y=10.6 g
Na2CO3溶液中溶质的质量分数为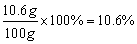
(本小问计算过程3分,计算结果1分)
解法二:Na2CO3 ~ CO2 (或写总反应式)……………………(1分)
106 44
x 4.4 g ……………………………………(1分)

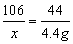 x=10.6 g…………………………(1分)
x=10.6 g…………………………(1分)
Na2CO3溶液中溶质的质量分数为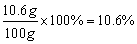 (1分)
(1分)
(其他合理解法同样给分)

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案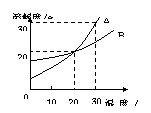
 和溶液,可以采取的措施是__________(答一条即可)。
和溶液,可以采取的措施是__________(答一条即可)。 质量分数的大小关系是____________。
质量分数的大小关系是____________。 B.
B.