题目内容
18.(1)现有$\stackrel{+1}{H}$、$\stackrel{+1}{Na}$、$\stackrel{+6}{S}$、$\stackrel{-2}{O}$四种元素,假定它们由两种或三种元素,按指定化合价形成化合物,按要求填写下列化学式和方程式:①金属氧化物Na2O; ②非金属氧化物H2O、SO3;③中和反应H2SO4+2NaOH=Na2SO4+2H2O.
(2)化肥厂用二氧化碳与氨气在一定条件下反应生成尿素[CO(NH2)2]和水的化学方程式为CO2+2NH3$\frac{\underline{\;一定条件\;}}{\;}$CO(NH2)2+H2O.
分析 (1)根据金属氧化物是氧化钠,非金属氧化物是水或三氧化硫,中和反应是酸和碱发生的反应进行分析;
(2)根据二氧化碳和氨气在一定条件下生成尿素和水进行分析.
解答 解:(1)金属氧化物是氧化钠,化学式为:Na2O,非金属氧化物是水或三氧化硫,化学式为:H2O、SO3,中和反应是酸和碱发生的反应,硫酸和氢氧化钠反应生成硫酸钠和水,化学方程式为:H2SO4+2NaOH=Na2SO4+2H2O;
(2)二氧化碳和氨气在一定条件下生成尿素和水,化学方程式为:CO2+2NH3$\frac{\underline{\;一定条件\;}}{\;}$CO(NH2)2+H2O.
故答案为:(1)Na2O,H2O、SO3,H2SO4+2NaOH=Na2SO4+2H2O;
(2)CO2+2NH3$\frac{\underline{\;一定条件\;}}{\;}$CO(NH2)2+H2O.
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.

练习册系列答案
相关题目
8.无色透明普通玻璃,其主要成分又称为钠钙玻璃,化学式为Na2CaSi6O14,其中硅元素的化合价为( )
| A. | +4 | B. | +3 | C. | +2 | D. | +1 |
9.化学变化的本质特征是( )
| A. | 发光放热 | B. | 有新物质生成 | ||
| C. | 有气体生成 | D. | 颜色、状态发生改变 |
6.工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4.为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析.
【资料1】草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4•3H2O$→_{△}^{浓H_{2}SO_{4}}$CO2↑+CO↑+4H2O
【资料2】浓硫酸具有吸水性;氢氧化钠溶液能吸收二氧化碳;碱石灰固体既能吸水又能吸收二氧化碳;CO能将FeO、Fe2O3、Fe3O4还原成铁.
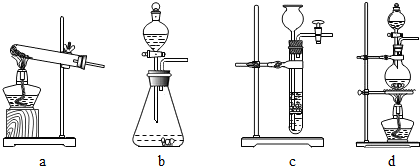
(1)下列可用作草酸分解制取气体的装置是d(填字母编号).
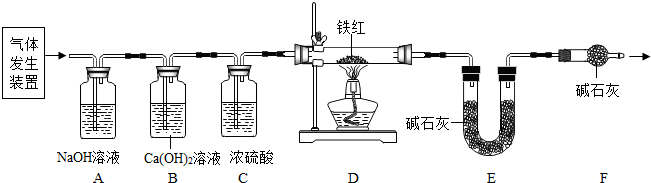
【问题讨论】用如图所示装置进行实验:
(2)实验前应先检查装置的气密性.
(3)B装置的作用是验证二氧化碳已除尽.
(4)对D装置加热前和停止加热后,都要通入过量的CO,其中加热前作用是:将装置中的空气排出,防止发生爆炸.
(5)写出D装置中所发生反应的一个化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
【数据分析】
【资料3】铁的常见氧化物中铁的质量分数:
(6)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①D中充分反应后得到Fe粉的质量为m g,则7.0<m<7.78.
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是76.0%.
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会偏小(填“偏小”、“不变”或“偏大”).
反思2:请指出【问题讨论】中实验装置的一个明显缺陷缺少尾气处理装置.
【拓展探究】用100t含氧化铁80%的赤铁矿石理论上可冶炼出含铁98%的生铁多少吨?(结果保留1为小数)
【资料1】草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4•3H2O$→_{△}^{浓H_{2}SO_{4}}$CO2↑+CO↑+4H2O
【资料2】浓硫酸具有吸水性;氢氧化钠溶液能吸收二氧化碳;碱石灰固体既能吸水又能吸收二氧化碳;CO能将FeO、Fe2O3、Fe3O4还原成铁.
(1)下列可用作草酸分解制取气体的装置是d(填字母编号).

【问题讨论】用如图所示装置进行实验:

(2)实验前应先检查装置的气密性.
(3)B装置的作用是验证二氧化碳已除尽.
(4)对D装置加热前和停止加热后,都要通入过量的CO,其中加热前作用是:将装置中的空气排出,防止发生爆炸.
(5)写出D装置中所发生反应的一个化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
【数据分析】
【资料3】铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
①D中充分反应后得到Fe粉的质量为m g,则7.0<m<7.78.
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是76.0%.
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会偏小(填“偏小”、“不变”或“偏大”).
反思2:请指出【问题讨论】中实验装置的一个明显缺陷缺少尾气处理装置.
【拓展探究】用100t含氧化铁80%的赤铁矿石理论上可冶炼出含铁98%的生铁多少吨?(结果保留1为小数)
13.完成元素周期表.
| 1 | 2 | ||||||
| 氢 H | 氦 He | ||||||
| 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 锂 Li | 铍 Be | 硼 B | 碳C | 氮 N | 氧O | 氟 F | 氖 Ne |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 钠Na | 镁Mg | 铝Al | 硅Si | 磷 P | 硫S | 氯Cl | 氩 Ar |
3.化学实验操作的规范性、安全性是实验成败的关键.下列实验操作中正确的是( )
| A. | 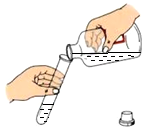 液体的倾倒 | B. | 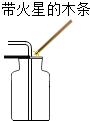 检验氧气是否集满 | ||
| C. |  给液体加热 | D. | 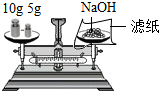 称取一定质量的NaOH |
2.我市启动了“生活垃圾分类”试点活动,对提升城市文明和生活质量具有积极的意义.下列各图为城市生活垃圾分类标志,则废旧电池属于( )
| A. |  可回收垃圾 | B. |  餐厨垃圾 | C. |  有害垃圾 | D. |  其他垃圾 |
19.水是最重要的自然资源,水资源不足,将严重影响人类生存.请结合下表回答:
(1)我国的人均水量约为2300m3/a,居世界第80几位,水资源紧缺程度轻度
(2)面临淡水资源的短缺,化学老师倡议“一水多用”.请你举出生活中的一项具体措施洗菜的水用来拖地等.
(3)为保护有限的水资源,在防止水污染的方面,你有什么好的建议和措施,试举两例对被污染的水进行处理使之符合排放标准、农业上提倡使用农家肥,合理使用化肥和农药.
| 水资源紧缺程度 | 轻度缺水 | 中度缺水 | 重度缺水 | 极度缺水 |
| 人均水量(m3/a) a为年的符号 | 1700-3000 | 1000-1700 | 500-1000 | <500 |
(2)面临淡水资源的短缺,化学老师倡议“一水多用”.请你举出生活中的一项具体措施洗菜的水用来拖地等.
(3)为保护有限的水资源,在防止水污染的方面,你有什么好的建议和措施,试举两例对被污染的水进行处理使之符合排放标准、农业上提倡使用农家肥,合理使用化肥和农药.