题目内容
8.下列是实验室常用的化学仪器.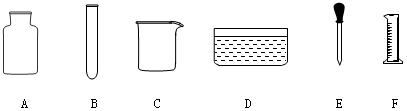
请用上图中所示的各种常用化学仪器的标号填空:
(1)少量试剂相互反应时用B;
(2)吸取和滴加少量液体时用E;
(3)收集和贮存少量气体时用A;
(4)量取一定体积液体药品时用EF;
(5)作配置溶液和较大量的反应容器用C.
分析 熟悉化学实验中的常用仪器和它们的作用即可顺利解答.
解答 解:(1)试管可作少量试剂的反应容器;
(2)胶头滴管可用来吸取和滴加少量液体;
(3)收集和贮存少量气体用集气瓶;
(4)量取一定体积的液体药品用量筒,接近刻度线时还要用胶头滴管;
(5)烧杯可用来配置溶液和作为较大量的物质的反应容器;
故答案为:(1)B; (2)E;(3)A;(4)E F;(5)C.
点评 了解常用仪器的名称和用途是解答此类题的基础和关键,属基础知识考查题.

练习册系列答案
相关题目
19.下面是某化学活动小组记录的实验现象,其中正确的是( )
| A. | 呼出气体中的水蒸气含量大于空气中水蒸气含量 | |
| B. | 硫酸铜溶液和氢氧化钠溶液反应后,蓝色固体减少至消失,形成蓝色溶液 | |
| C. | 试管中的水沸腾时,看见试管口产生白雾 | |
| D. | 大理石和稀盐酸反应时,可以看到固体表面有二氧化碳气体冒出 |
16.已知下列4个反应在一定条件下都能发生,其中属于化合反应的是( )
| A. | 氧化汞→汞+氧气 | |
| B. | 硫+氧气→二氧化硫 | |
| C. | 石灰水+盐酸→氯化钙+二氧化碳+水 | |
| D. | 硫酸铜+氢氧化钠→氢氧化铜+硫酸钠 |
3.下列物质中不能造成空气污染的是( )
| A. | 二氧化氮 | B. | 可吸入颗粒 | C. | 二氧化硫 | D. | 二氧化碳 |
17.下列各项中属于化学学科研究内容的是( )
| A. | 培育新品种,增加农作物的产量 | B. | 利用指南针确定方向 | ||
| C. | 综合利用石油生产优良人造纤维 | D. | 设计新程序、开发计算机新功能 |
18.某化学兴趣小组的同学利用过氧化氢分解来探究影响化学反应速率的因素,他们设计如表的实验,并记录了相关数据:
(1)在上述实验中二氧化锰起催化作用.
(2)写出该实验涉及反应的文字表达式:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(3)通过实验①②对比可知,化学反应速率与过氧化氢浓度有关;从实验②③对比可知,化学反应速率与温度有关.
(4)同学们设计了如图1所示的装置进行实验,其中量筒的作用是根据进入量筒中水的体积判断生成的氧气的体积;在第四组实验中,出现了胶塞弹飞和试剂喷出的现象,导致该现象出现的原因可能是过氧化氢浓度越大则反应越剧烈(答案合理即可).
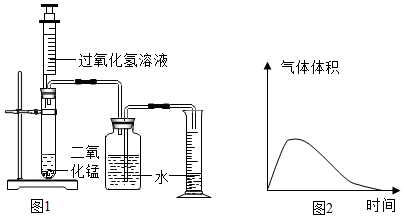
(5)实验过程中同学们发现很难控制反应的温度,反应进行一段时间后溶液的温度总是比起始温度高,说明该反应放出热量.
(6)同学们通过记录并分析实验数据发现,过氧化氢分解的速率先增大后减小,如图2所示.请你帮他们解释其原因:反应放热能加快反应,随着反应的进行过氧化氢浓度降低,反应逐渐减慢.过氧化氢分解的快慢还可能受哪些因素影响呢?请你再举出两种因素:催化剂的种类;;催化剂的颗粒大小(催化剂的用量、是否用催化剂等).
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/mL | 二氧化锰的用量/g | 温度/℃ | 收集氧气的体积/mL | 反应所需的时间/s |
| ① | 5 | 2 | 0.1 | 20 | 20 | 48 |
| ② | 10 | 2 | 0.1 | 20 | 20 | 30 |
| ③ | 10 | 2 | 0.1 | 40 | 20 | 18 |
| ④ | 2 | 0.1 | 60 | 20 | 6 |
(2)写出该实验涉及反应的文字表达式:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(3)通过实验①②对比可知,化学反应速率与过氧化氢浓度有关;从实验②③对比可知,化学反应速率与温度有关.
(4)同学们设计了如图1所示的装置进行实验,其中量筒的作用是根据进入量筒中水的体积判断生成的氧气的体积;在第四组实验中,出现了胶塞弹飞和试剂喷出的现象,导致该现象出现的原因可能是过氧化氢浓度越大则反应越剧烈(答案合理即可).

(5)实验过程中同学们发现很难控制反应的温度,反应进行一段时间后溶液的温度总是比起始温度高,说明该反应放出热量.
(6)同学们通过记录并分析实验数据发现,过氧化氢分解的速率先增大后减小,如图2所示.请你帮他们解释其原因:反应放热能加快反应,随着反应的进行过氧化氢浓度降低,反应逐渐减慢.过氧化氢分解的快慢还可能受哪些因素影响呢?请你再举出两种因素:催化剂的种类;;催化剂的颗粒大小(催化剂的用量、是否用催化剂等).
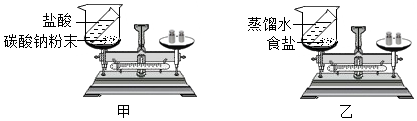
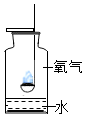 如图,老师在实验室给学生做氧气性质的演示实验图.
如图,老师在实验室给学生做氧气性质的演示实验图.