题目内容
14.根据下列粒子的结构示意图,回答下列问题: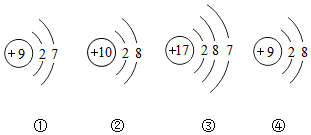
(1)表示同种元素的粒子是①④(填序号).
(2)在化学反应中容易得到电子的粒子是①③(填序号).
(3)随着“神舟六号”的发射成功,我国还将发射绕月探测卫星.其任务之一是寻找一种新能源--氦-3,氦-3原子核是由一个中子和两个质子构成的,其原子核外电子数为2,其相对原子质量为3.
分析 (1)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的是核电荷数(即核内质子数),据此进行分析解答.
(2)若原子的最外层电子数≥4,在化学反应中易得电子,据此进行分析解答.
(3)根据原子中:核电荷数=核内质子数=核外电子数,相对原子质量=质子数+中子数,结合题意进行分析解答.
解答 解:(1)根据决定元素种类的是核电荷数(即核内质子数),因为①④的核内质子数相同,所以①④属于同种元素的粒子.
(2)①③的最外层电子数均为7,均大于4,均在化学反应中易得到1个电子而形成阴离子.
(3)因为原子中:核电荷数=核内质子数=核外电子数,由题意氦-3原子的原子核中含有2个质子,故其原子核外电子数为为2.
相对原子质量=质子数+中子数,氦-3原子核是由一个中子和两个质子构成的,则其相对原子质量为2+1=3.
故答案为:(1)①④;(2)①③;(3)2;3.
点评 本题难度不大,解题的关键是掌握并灵活运用原子结构示意图的含义、原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数.

练习册系列答案
相关题目
5.2015年中国科学家屠呦呦因青蒿素(C15H22O5)和双氢青蒿素(C15H24O5)而荣获了诺贝尔奖.下列有关说法中正确的是( )
| A. | 青蒿素比双氢青蒿素少两个氢原子 | |
| B. | 双氢青蒿素的相对分子质量为284g | |
| C. | 两种分子中碳、氧原子个数比都为3:1 | |
| D. | 1个青蒿素分子中含有11个氢分子 |
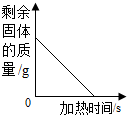
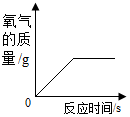
 如图是西餐中非常好喝的罗宋汤.请回答问题:
如图是西餐中非常好喝的罗宋汤.请回答问题: 2MgO B、CaO+H2O═Ca(OH)2 C、2H2O
2MgO B、CaO+H2O═Ca(OH)2 C、2H2O 2H2↑+O2↑
2H2↑+O2↑ CaO+CO2↑ E、H2+CuO
CaO+CO2↑ E、H2+CuO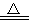 Cu+H2O F、HCl+NaOH═NaCl+H2O
Cu+H2O F、HCl+NaOH═NaCl+H2O