题目内容
9.下列与实验操作或离子检验有关的说法正确的是( )| A. | 称量一定质量NaCl固体时,没有用烧杯,直接放在右盘的滤纸上 | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42ˉ | |
| C. | 蒸发时,待水分完全蒸干后才能停止加热 | |
| D. | 加入硝酸酸化的硝酸钡溶液既无沉淀又无气体产生,再加入硝酸银溶液,立刻产生白色沉淀,一定有Clˉ |
分析 A.固体在左盘中称量;
B.沉淀可能为AgCl;
C.蒸发时可利用余热加热;
D.硝酸排除其它离子的干扰,再加硝酸银生成沉淀为AgCl.
解答 解:A.固体在左盘中称量,称量操作不合理,故A错误;
B.沉淀可能为AgCl,应先加盐酸,再加氯化钡,故B错误;
C.蒸发时可利用余热加热,不能完全蒸干,故C错误;
D.硝酸排除其它离子的干扰,再加硝酸银生成沉淀为AgCl,则氯离子检验的操作、现象、结论均合理,故D正确;
故选D.
点评 本题考查物质的鉴别和检验,为高频考点,把握物质的性质及性质差异为解答的关键,侧重分析与实验基本操作能力的考查,题目难度不大.

练习册系列答案
相关题目
19.做完“铁在氧气里燃烧”实验后,小明同学有两个疑惑不解的问题,于是他进行了以下探究活动,请你一同参与.
[问题1]铁燃烧时溅落下来的黑色物质中还有没有铁呢?
[查阅资料1]
(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
(2)铁的氧化物均能溶于酸的溶液.
[实验探究]
将冷却后的黑色物质碾碎,装入试管,加入稀盐酸溶液,观察到的现象是产生气泡,说明铁燃烧时溅落下来的黑色物质中还含有铁.
[问题2]铁燃烧的产物为什么不是Fe2O3呢?
[查阅资料2]
(1)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
(2)Fe2O3高温时分解成Fe3O4.
[理论探讨]
根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在1400℃~1538℃之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产生是Fe3O4.
[拓展延伸]
(1)实验中为了防止集气瓶炸裂,必须在集气瓶底部铺一层细沙,或加入适量的水.
(2)Fe2O3高温时会分解成Fe3O4和一种气体,请写出此反应的化学方程式6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑.
(3)有些超市的食品密封包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色由黑色变成红棕色,就说明包装盒破损进气,这样售货员就能及时发现并处理.
[问题1]铁燃烧时溅落下来的黑色物质中还有没有铁呢?
[查阅资料1]
(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
(2)铁的氧化物均能溶于酸的溶液.
[实验探究]
将冷却后的黑色物质碾碎,装入试管,加入稀盐酸溶液,观察到的现象是产生气泡,说明铁燃烧时溅落下来的黑色物质中还含有铁.
[问题2]铁燃烧的产物为什么不是Fe2O3呢?
[查阅资料2]
(1)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
[理论探讨]
根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在1400℃~1538℃之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产生是Fe3O4.
[拓展延伸]
(1)实验中为了防止集气瓶炸裂,必须在集气瓶底部铺一层细沙,或加入适量的水.
(2)Fe2O3高温时会分解成Fe3O4和一种气体,请写出此反应的化学方程式6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑.
(3)有些超市的食品密封包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色由黑色变成红棕色,就说明包装盒破损进气,这样售货员就能及时发现并处理.
20.取4份等质量的KClO3,向其中3份中分别加入少量等质量的KMnO4、MnO2和Mn,分别在某温度下加热至质量不再改变,测定产生氧气的质量.然后将剩余固体溶于足量水中,添加过少量物质的组别中均有相同组成的不溶物.测定结果如表:
已知ml>m2>m3,下列关于此实验的说法一定正确的是( )
| 组别 | ① | ② | ③ | ④ |
| 加入物质 | 无 | KMnO4 | MnO2 | Mn |
| 产生氧气的质量/g | 0 | ml | m2 | m3 |
| 不溶物的质量/g | 0 | wl | w2 | w3 |
| A. | 残留不溶性物质的质量关系为w1>w2>w3 | |
| B. | 不加入其他物质时,KClO3未发生分解反应 | |
| C. | KMnO4是KClO3分解制氧气效果最好的催化剂 | |
| D. | 3种物质的加入都有利于KClO3分解制氧气 |
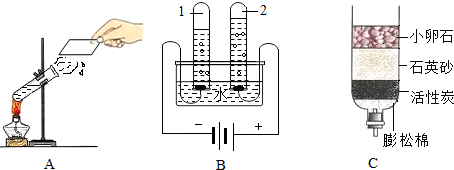
4.仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置(图1、图2)就能实现相应实验目的是( )
| 选项 | A | B | C | D |
| 实验项目 | 除去KCl中少量的MnO2 | 用10mol/L的盐酸配制100mL0.1mol/L的盐酸 | 用氯化钠溶液制备氯化钠晶体 | 除去CO2气体中的HCl |
| 实验仪器 或装置 | 烧杯、玻璃棒、分液漏斗 | 100mL容量瓶、玻璃棒、烧杯 | 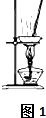 | 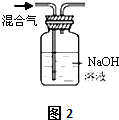 |
| A. | A | B. | B | C. | C | D. | D |
14.实验室进行NaCl溶液蒸发时,一般有以下操作过程,其正确的操作顺序是( )
①放置酒精灯 ②固定铁圈的位置 ③放上蒸发皿 ④加热搅拌 ⑤停止加热、余热蒸干.
①放置酒精灯 ②固定铁圈的位置 ③放上蒸发皿 ④加热搅拌 ⑤停止加热、余热蒸干.
| A. | ①②③④ | B. | ①②③④⑤ | C. | ②③①④⑤ | D. | ②①③④⑤ |
1.学校食堂提供了下列5种食物:①青菜②苹果③米饭④猪肉⑤鱼.较合理的组合是( )
| A. | ①②③ | B. | ①③⑤ | C. | ①④⑤ | D. | ③④⑤ |
18.2016年“世界环境日”中国主题为“改善环境质量,推动绿色发展”.下列做法不符合该主题的是( )
| A. | 推广公共自行车项目,为人们绿色出行提供便利 | |
| B. | 用天然气替代煤、液化石油气,减少酸雨的形成 | |
| C. | 大量焚烧秸秆,减少农村秸秆堆放问题 | |
| D. | 大力开发氢能、太阳能,减少化石燃料燃烧 |