题目内容
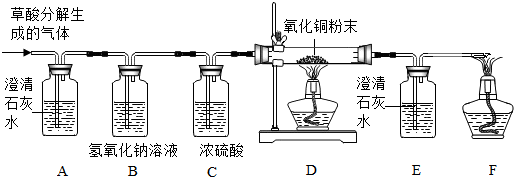
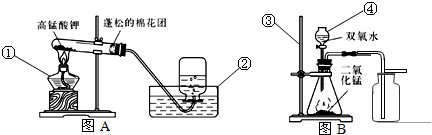
某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如图所示.请回答有关问题:

(1)为避免一氧化碳污染空气,并回收利用一氧化碳,方框中连接的是C和D,导管接口的连接顺序为a→ → → .C装置中NaOH的作用是 .
(2)实验开始时,应 (填“先加热再通CO”或“先通CO再加热”),目的是 .
(3)实验进行一段时间后,玻璃管A中出现的现象为 ,反应方程式为 ;B中出现的现象为
,反应的化学反应方程式为 .
(4)除CO外,还有哪些物质可以还原Fe2O3 (请写一物质的化学式).

(1)为避免一氧化碳污染空气,并回收利用一氧化碳,方框中连接的是C和D,导管接口的连接顺序为a→
(2)实验开始时,应
(3)实验进行一段时间后,玻璃管A中出现的现象为
(4)除CO外,还有哪些物质可以还原Fe2O3
考点:一氧化碳还原氧化铁,常见气体的检验与除杂方法,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:只有熟悉一氧化碳与氧化铁反应的生成物、实验装置、实验现象、一氧化碳的化学性质和污染及能源的再利用等知识,才能正确解答本题.
解答:解:(1)一氧化碳有毒,不能够直接排放到空气中去,要把一氧化碳收集起来,所以导管接口的连接顺序为b、d、e,排出的氢氧化钠溶液流到D中的烧杯中去.C装置中NaOH的作用是吸收B中没反应掉的二氧化碳;
(2)因为一氧化碳具有可燃性,能和氧气混合在点燃的条件下会发生爆炸,所以实验开始时应先通一氧化碳再加热,目的是赶尽玻璃管内的空气,防止加热爆炸;
(3)氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳,氧化铁是红棕色的,铁粉是黑色的,故玻璃管A中出现的现象为:固体由红棕色变成黑色,反应方程式为:3CO+Fe2O3
2Fe+3CO2;B中澄清的石灰水变浑浊,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;
(4)除CO外,还具有还原性的物质有C或H2.
故答案为:(1)b;d;除去残余的二氧化碳;(2)先通CO再加热;赶尽玻璃管内的空气,防止加热爆炸;(3)固体由红棕色变成黑色;3CO+Fe2O3
2Fe+3 CO2;澄清的石灰水变浑浊;CO2+Ca(OH)2═CaCO3↓+H2O;(4)C.
(2)因为一氧化碳具有可燃性,能和氧气混合在点燃的条件下会发生爆炸,所以实验开始时应先通一氧化碳再加热,目的是赶尽玻璃管内的空气,防止加热爆炸;
(3)氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳,氧化铁是红棕色的,铁粉是黑色的,故玻璃管A中出现的现象为:固体由红棕色变成黑色,反应方程式为:3CO+Fe2O3
| ||
(4)除CO外,还具有还原性的物质有C或H2.
故答案为:(1)b;d;除去残余的二氧化碳;(2)先通CO再加热;赶尽玻璃管内的空气,防止加热爆炸;(3)固体由红棕色变成黑色;3CO+Fe2O3
| ||
点评:本题主要考查一氧化碳与氧化铁反应实验装置、实验现象、一氧化碳的化学性质和污染及能源的再利用,难度稍大.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
制100g质量分数为10%的氯化钠溶液,下列操作导致质量分数变大的是( )
| A、把配好的溶液装入试剂瓶时部分溶液洒出 |
| B、用量筒量取90mL水时俯视读数 |
| C、食盐中含有杂质 |
| D、用蒸馏水润洗用于溶解氯化钠的烧杯 |
将下列各组物质分别放入水中,有化学反应发生,但既无沉淀生成,又无气体放出的是( )
| A、CaCl2、KOH、Na2C03 |
| B、Na2C03、BaCl2、HCl |
| C、K2SO4、HCl、NaOH |
| D、CuS04、HCl、NaCl |
某铁的氧化物中,铁元素与氧元素质量比为21:8,则该氧化物的相对分子质量是( )
| A、72 | B、160 |
| C、232 | D、288 |
 A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答:
A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答: