题目内容
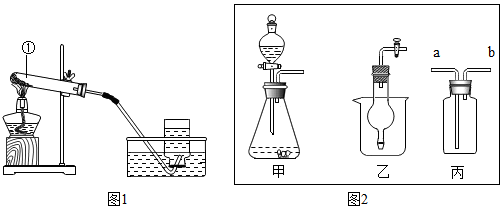
8.通过一学期的化学学习,同学们对实验室制取气体有了一定认识.(1)若用如图1装置加热高锰酸钾制取氧气:则发生反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;写出标号仪器①的名称试管;实验结束,停止加热时要先把导管移出水面,其目的是为防止水倒流入试管,引起试管的炸裂.
(2)若分解过氧化氢制取氧气,供选用的装置如图2,要得到平稳的氧气流,应选用的发生装置是甲;若用丙装置收集较纯净的氧气,应先在丙中装入水,再将氧气从a端导入.
分析 (1)根据反应物、反应条件、生成物写出反应的方程式;以及常见仪器的名称以及氧气制取的注意事项进行解答;
(2)根据注射器可控制注入双氧水的速度,即可控制反应速率使气流产生的平稳;浓硫酸具有吸水性,能够干燥氧气.
解答 解:(1)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;仪器的名称:①试管;为防止水倒流入试管,引起试管的炸裂,实验结束,停止加热时要先把导管移出水面;
(2)用乙装置分解过氧化氢时,反应速率由快到慢;用甲装置分解过氧化氢时,过氧化氢溶液可以由注射器均匀地加入,反应速率变化不大,能够得到平稳的氧气流;若用丙装置收集较纯净的氧气,应先在丙中装入水,氧气的密度比水的小,再将氧气从a端导入.
故答案为:
(1)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;试管;防止水倒流入试管,引起试管的炸裂;
(2)甲;水;a.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
相关题目
16.“低碳生活”是指在生活作息时减少能量耗用,使二氧化碳排放降低的一种时尚生活方式,下列不符合“低碳生活”主题的是( )
| A. | 参加“地球熄灯一小时”活动 | B. | 秋天焚烧落叶 | ||
| C. | 开发回收利用二氧化碳新技术 | D. | 用旧报纸制铅笔杆 |
3.中华炭雕(主要成分为木炭),是集观赏与空气净化于一体的工艺品,下列说法错误的是( )
| A. | 炭雕吸附有害气体是物理变化 | B. | 炭雕内部具有疏松多孔的结构 | ||
| C. | 炭雕是质地透明的固体 | D. | 炭雕具有可燃性 |
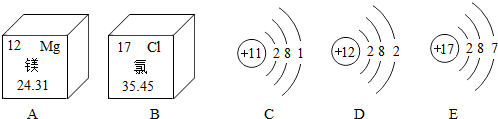
20.市场上有“高钙牛奶”、“含氟牙膏”等商品,商品名中的“钙、氟”指的是( )
| A. | 元素 | B. | 分子 | C. | 单质 | D. | 原子 |
17.放入水中不能形成溶液的物质是( )
| A. | 白酒 | B. | 食盐 | C. | 白糖 | D. | 植物油 |
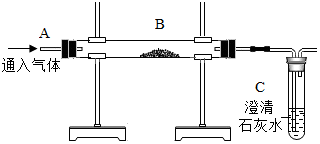 用如图装置完成以下实验:
用如图装置完成以下实验: