题目内容
实验室常利用以下装置完成气体制备及性质实验.请回答:

(1)指出编号仪器的名称:① ,② .
(2)以上A装置有一处明显的错误,请加以改正 .利用改正后的装置继续完成后面的实验.
(3)欲使用高锰酸钾制取氧气,应选择的发生装置是 (填字母).
(4)运用B装置也可以制取氧气,请用化学方程式表示 .
(5)实验室可以用大理石和稀盐酸来制取某种气体,应选用的发生装置为 .反应原理用化学方程式表示为 + ,欲收集该气体,应选择的装置是 (填序号).验满的方法是 .若将该气体通入澄清石灰水中,观察到的现象是 ,请用化学方程式进行解释该现象 .
(6)氨气在通常状况下是一种无色、有刺激性趣味的气体,密度比空气小,极易溶于水.实验室用加热氯化铵和熟石灰两种固体混合物制取氨气.则发生装置可选用 ,收集装置可选用 .请配平实验室制氨气的化学方程式
NH4Cl+ Ca(OH)2 CaCl2+ H2O+ NH3 ↑ .
CaCl2+ H2O+ NH3 ↑ .
【考点】常用气体的发生装置和收集装置与选取方法;实验室制取氧气的反应原理;二氧化碳的实验室制法;二氧化碳的检验和验满;化学方程式的配平;书写化学方程式、文字表达式、电离方程式.
【专题】化学用语和质量守恒定律;常见仪器及化学实验基本操作;常见气体的实验室制法、检验、干燥与净化.
【分析】(1)根据实验室常用仪器分析解答;
(2)根据A装置制取气体的注意事项进行分析;
(3)根据高锰酸钾制取氧气的反应物是固体,反应条件是加热,属于固体加热型解答;
(4)B装置是固液混合制取气体,过氧化氢在二氧化锰的催化作用下生成水和氧气可用此发生装置,据反应原理书写方程式;
(5)实验室用大理石和稀盐酸反应制取二氧化碳不需加热,属于固液常温型,故选发生装置B,大理石主要成分碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,二氧化碳密度比空气大,能溶于水,所以用向上排空气法收集;验满二氧化碳的方法是将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断;二氧化碳和石灰水的主要成分氢氧化钙反应生成碳酸钙沉淀和水;
(6)根据实验室制取氨气的反应物是固体,反应条件是加热,氨气密度比空气小,极易溶于水,化学反应恰好原子的种类和数目不变进行分析.
【解答】解:(1)图中标号仪器分别是酒精灯,长颈漏斗;
(2)A装置有一处明显的错误,装置A中导管伸入试管太长,不利于气体导出、透过橡胶塞即可;
(3)高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以应选择的发生装置是A;
(4)B装置是固液混合制取气体,过氧化氢在二氧化锰的催化作用下生成水和氧气可用此发生装置,化学方程式为:2H2O2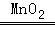 2H2O+O2↑;
2H2O+O2↑;
(5)实验室用大理石和稀盐酸反应制取二氧化碳,反应物是固体和液体,反应条件是常温,所以应选用的发生装置为B,大理石主要成分碳酸钙和盐酸反应生成氯化钙、水和二 氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,二氧化碳密度比空气大,能溶于水,所以应选择的装置是E,二氧化碳不具有助燃性,所以验满的方法是:将燃着的木条放在集气瓶口,木条熄灭,证明集满,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以观察到的现象是:澄清石灰水变浑浊,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,二氧化碳密度比空气大,能溶于水,所以应选择的装置是E,二氧化碳不具有助燃性,所以验满的方法是:将燃着的木条放在集气瓶口,木条熄灭,证明集满,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以观察到的现象是:澄清石灰水变浑浊,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(6)实验室制取氨气的反应物是固体,反应条件是加热,所以发生装置可选用A,氨气密度比空气小,极易溶于水,所以只能用向下排空气法收集,收集装置选用D,氯化铵和氢氧化钙在加热的条件下反应生成氯化钙、水和氨气,据反应前后原子的种类和数目不变,可知化学方程式为:2NH4Cl+Ca(OH)2 CaCl2+2H2O+2NH3↑.
CaCl2+2H2O+2NH3↑.
故答案为:(1)酒精灯;长颈漏斗;
(2)导管伸入试管太长、透过橡胶塞即可;
(3)A;
(4)2H2O2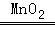 2H2O+O2↑;
2H2O+O2↑;
(5)B;CaCO3+2HCl=CaCl2+H2O+CO2↑;E;将燃着的木条放在集气瓶口,木条熄灭,证明集满;澄清石灰水变浑浊;Ca(OH)2+CO2=CaCO3↓+H2O;
(6)A;D;2NH4Cl+Ca(OH)2 CaCl2+2H2O+2NH3↑.
CaCl2+2H2O+2NH3↑.
【点评】本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择,并能据题意灵活分析解答.

下列关于混合物、酸、碱、盐、氧化物分类完全正确的是( )
| 混合物 | 酸 | 碱 | 盐 | 氧化物 | |
| A | 冰水混合物 | 硫酸 | 氢氧化钠 | 硫酸钡 | 干冰 |
| B | 焦炉煤气 | 硝酸 | 氢氧化钙 | 碳酸氢钙 | 四氧化三铁 |
| C | 合金 | 盐酸 | 碱式碳酸铜 | 氯化银 | 一氧化碳 |
| D | 空气 | 醋酸 | 氢氧化钡 | 碳酸钙 | 氯酸钾 |
A.A B.B C.C D.D

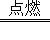 2CO2”的质量关系,不正确的是( )
2CO2”的质量关系,不正确的是( )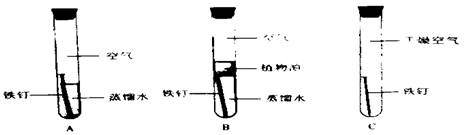
 该兴趣小组将洁净无锈的铁钉分别置于上图所示装置中,经过一段时间观察 ,(填装置序号)装置中出现了明显的锈迹。
该兴趣小组将洁净无锈的铁钉分别置于上图所示装置中,经过一段时间观察 ,(填装置序号)装置中出现了明显的锈迹。