题目内容
20g 20%的NaOH溶液与20g 20%的H2SO4溶液充分反应后,滴入紫色石蕊试液显( )
| A、紫色 | B、蓝色 | C、红色 | D、无色 |
考点:中和反应及其应用,酸碱指示剂及其性质,根据化学反应方程式的计算
专题:常见的酸 酸的通性
分析:根据氢氧化钠与硫酸反应的化学方程式,判断完全反应后剩余的是哪一种溶液,再根据紫色石蕊试液遇酸变红色,遇碱变蓝色,遇中性溶液不变色,进行分析判断.
解答:解:20克20%的氢氧化钠溶液和20克20%的硫酸溶液中,所含溶质的质量均为20g×20%=4g.
反应中消耗硫酸与氢氧化钠的质量比关系如下:
H2SO4+2NaOH═Na2SO4+2H2O
98 80
可知,98份质量的硫酸与80份质量的氢氧化钠恰好完全反应,则20克20%的氢氧化钠溶液和20克20%的硫酸溶液混合充分反应后,氢氧化钠有剩余,溶液显碱性,最终混合后的液体呈蓝色.
故选:B.
反应中消耗硫酸与氢氧化钠的质量比关系如下:
H2SO4+2NaOH═Na2SO4+2H2O
98 80
可知,98份质量的硫酸与80份质量的氢氧化钠恰好完全反应,则20克20%的氢氧化钠溶液和20克20%的硫酸溶液混合充分反应后,氢氧化钠有剩余,溶液显碱性,最终混合后的液体呈蓝色.
故选:B.
点评:本题难度不大,掌握中和反应应用,根据化学方程式的计算判断出反应后剩余的物质是正确解答本题的关键.

练习册系列答案
相关题目
“人造空气”帮助人类实现了“太空漫步”的梦想,其中含有70%的 N2、20%以上的O2、还有CO2和稀有气说法不正确体等.下列说法不正确的是( )
| A、燃着的蜡烛在“人造空气”中会熄灭 | ||||
| B、“人造空气”比空气中的氮气含量低 | ||||
C、可以利用反应4P+5O2
| ||||
| D、“人造空气”的组成与实际生活中空气的组成有区别 |
能在溶液中大量共存,且溶液为无色透明的一组物质是( )
| A、FeCl3、CuSO4、NaCl |
| B、BaCl2、Na2SO4、NaOH |
| C、CaCl2、Na2CO3、AgNO3 |
| D、K2SO4、NaNO3、KCl |
有一瓶无色液体X,分成等量的三份,向其中分别加入少量的稀盐酸、氢氧化钠溶液、硝酸钡溶液,产生的现象如下表.则该无色液体X是下列各项中的( )
| 加入物质 | 稀盐酸 | 氢氧化钠溶液 | 硝酸钡溶液 |
| 现象 | 无明显现象 | 刺激性气味的气体 | 出现白色沉淀 |
| A、氯化钙溶液 |
| B、硫酸铵溶液 |
| C、碳酸钠溶液 |
| D、氯化钠溶液 |
下列所示的图象不能反映对应实验的是( )
A、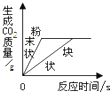 等质量的碳酸钙分别与等体积等质量分数的足量稀盐酸反应 |
B、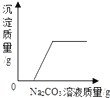 向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液 |
C、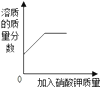 某温度,向一定量饱和硝酸钾溶液中加入硝酸钾晶体 |
D、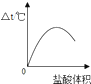 向一定体积的氧氧化钠溶液中加入足量的稀盐酸 |
在由分子构成的物质中,下列说法正确的是( )
| A、由不同种分子构成的物质一定是混合物 |
| B、混合物不一定由不同种分子构成 |
| C、纯净物不一定由同种分子构成 |
| D、由同种分子构成物质不一定是纯净物 |
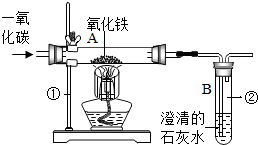
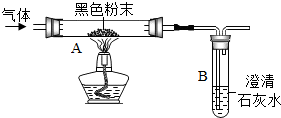 类比法是化学研究物质的重要方法之一.草酸[H2C2O4]的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究:
类比法是化学研究物质的重要方法之一.草酸[H2C2O4]的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究: