题目内容
11.下列四个实验方案设计不合理的是( )| 选项 | 实验目的 | 方案 |
| A | 鉴别硝酸钠溶液和硫酸钾溶液 | 取样,滴加Ba(NO3)2溶液,观察现象 |
| B | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、蒸发 |
| C | 除去CaO中的CaCO3 | 高温加热到固体质量不变 |
| D | 探究Mg、Ag、Cu金属的 活动性顺序 | 将两根光亮的镁条分别伸入 硫酸铜溶液和硝酸银溶液中 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据两种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质与同种物质反应的现象相同,则无法鉴别它们.
B、根据粗盐提纯是将粗盐中含有的泥沙等不溶物除去,进行分析判断.
C、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
D、在金属活动性顺序中,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,进行分析判断.
解答 解:A、硫酸钾溶液能与Ba(NO3)2溶液反应生成硫酸钡沉淀和硝酸钾,硝酸钠溶液与Ba(NO3)2溶液不反应,不能鉴别,故选项实验方案设计合理.
B、粗盐的主要成分是氯化钠,粗盐提纯是通过将粗盐研碎、溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐)得到精盐的过程,故选项实验方案设计合理.
C、CaCO3固体高温煅烧生成氧化钙和二氧化碳,加热到固体质量不变,能除去杂质且没有引入新的杂质,符合除杂原则,故选项实验方案设计合理.
D、将两根光亮的镁条分别伸入硫酸铜溶液和硝酸银溶液中,镁均能与硫酸铜溶液、AgNO3反应置换出铜、银,说明了活动性Mg>Ag,Cu>Ag;无法比较镁和铜的金属活动性,故选项实验方案设计不合理.
故选:D.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体解题时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1. 实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
【实验原理】由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测量结果与理论值误差较大.
【实验改进】
Ⅰ.根据铁在空气中生锈的原理设计如图实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
【交流表达】
(1)红磷在氧气中燃烧的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
根据表中数据计算,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%).
(2)从实验原理角度分析,改进后的结果比教材实验准确度髙的原因是铁生锈消耗氧气更彻底(写一条)
 实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
实验室用红磷燃烧来粗略测定空气中氧气含量的装置.【实验原理】由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测量结果与理论值误差较大.
【实验改进】
Ⅰ.根据铁在空气中生锈的原理设计如图实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
(1)红磷在氧气中燃烧的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
根据表中数据计算,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%).
(2)从实验原理角度分析,改进后的结果比教材实验准确度髙的原因是铁生锈消耗氧气更彻底(写一条)
19.氧气是空气的主要成分之一,有关氧气说法错误的是( )
| A. | 铁丝能在氧气中燃烧,火星四溅,产生黑色固体 | |
| B. | 氧气在低温高压下能变为液体或固体 | |
| C. | 用带火星的木条可以检验氧气 | |
| D. | 鱼类能在水中生活,证明氧气易溶于水 |
6.以下实验装置中不能用来证明质量守恒定律的是( )
| A. | 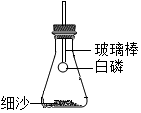 | B. | 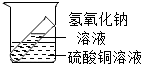 | C. | 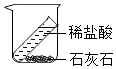 | D. | 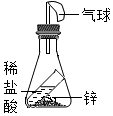 |
16.下列说法不正确的是( )
| A. | 化学式都是由化合价得出来的 | |
| B. | 在化合物中,各元素的正负化合价的代数和一定为零 | |
| C. | 硝酸铵(NH4NO3)中氮既显-3价,又显+5价 | |
| D. | 氢气中氢元素的化合价为0价 |
1.2015 年我国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素而获得诺贝尔生理学或医学奖.请回答问题:
(1)已知青蒿素的化学式为C15H22O5,则下列说法正确的是AB.
A.青蒿素属于有机化合物
B.一个青蒿素分子中含有42 个原子
C.青蒿素的含碳量为28.4%
D.青蒿素中C、H、O 三种元素的质量比为15:22:5
(2)早在东晋时期,葛洪的著作《肘后备急方》中就有抗疟法“青蒿一握,以水二升渍,绞取汁,尽服之”的记载.屠呦呦受此启发,提出把黄花蒿浸泡在低沸点的乙醚中(沸点为35℃)加热煮沸来提取青蒿素,从而避免了传统的高温水煎易破坏青蒿素的弊端.为什么此法可避免高温破坏青蒿素?请对此作出解释.乙醚沸点低,当加热到35℃时就会汽化带走热量,温度不能持续升高,就不会破坏青蒿素.
(3)某兴趣小组的同学在同一地点采集黄花蒿的根、茎、叶(叶龄7 天),共采集3 次,并测定样品中青蒿素的含量,记录入下表.
请补充完整表格内的栏目:此实验的研究目的是研究比较植物根茎叶三个部位中青蒿素的含量.
(1)已知青蒿素的化学式为C15H22O5,则下列说法正确的是AB.
A.青蒿素属于有机化合物
B.一个青蒿素分子中含有42 个原子
C.青蒿素的含碳量为28.4%
D.青蒿素中C、H、O 三种元素的质量比为15:22:5
(2)早在东晋时期,葛洪的著作《肘后备急方》中就有抗疟法“青蒿一握,以水二升渍,绞取汁,尽服之”的记载.屠呦呦受此启发,提出把黄花蒿浸泡在低沸点的乙醚中(沸点为35℃)加热煮沸来提取青蒿素,从而避免了传统的高温水煎易破坏青蒿素的弊端.为什么此法可避免高温破坏青蒿素?请对此作出解释.乙醚沸点低,当加热到35℃时就会汽化带走热量,温度不能持续升高,就不会破坏青蒿素.
(3)某兴趣小组的同学在同一地点采集黄花蒿的根、茎、叶(叶龄7 天),共采集3 次,并测定样品中青蒿素的含量,记录入下表.
| 青蒿素含量(mg/g) | ||||
| 第1次 | 第2次 | 第3次 | ||
| 根 | 1.02 | 1.05 | 1.14 | |
| 茎 | 0.09 | 0.11 | 0.10 | |
| 叶(叶龄7天) | 4.57 | 4.65 | 4.58 | |

 能源-国家发展的关键.近年来,我国不但在“一带一路”战略推进了能源的国际合作,还在今年的5月18日于南海取得了可燃冰试开采的成功!请回答:
能源-国家发展的关键.近年来,我国不但在“一带一路”战略推进了能源的国际合作,还在今年的5月18日于南海取得了可燃冰试开采的成功!请回答: