题目内容
9.化学调研小组的同学用氢氧化钠和盐酸探究中和反应,也请你参加.(1)甲组同学用一瓶稀氢氧化钠溶液进行实验时,当往烧杯中滴加稀盐酸时,发现有少量的气泡冒出,小组同学根据这一现象进行讨论,一致认为其原因可能是稀氢氧化钠溶液已经变质,变质的原因是(用化学方程式解释)CO2+2NaOH═Na2CO3+H2O.由此,同学们建议实验室保存氢氧化钠时应注意密封保存.为了除去稀氢氧化钠溶液中变质产生的碳酸钠,你认为可选用下列物质中的A(填序号).
A.饱和氢氧化钙溶液 B.稀盐酸 C.氯化钙溶液 D.氯化钠溶液
(2)乙组同学计划借助酚酞溶液继续研究氢氧化钠溶液与盐酸的反应.他们向烧杯里的稀氢氧化钠溶液中滴加稀盐酸一定量后,发现忘记了滴加酚酞溶液.于是,小组的同学从烧杯中取少量反应后的溶液M于一支试管中,并向试管中滴加几滴酚酞溶液,振荡,观察到酚酞溶液不变色.于是他们得出了“两种物质已恰好完全中和”的结论.你认为他们这样得出的结论是错误(填“正确”或“错误”)的,理由是:盐酸过量,溶液显酸性,酚酞溶液也不变色.
请你帮助乙组的同学,设计一个实验探究反应后溶液M的酸碱性.现有A.Cu片、B.Fe片、C.NaHCO3溶液、D.MgCl2溶液、E.CuO等五种物质,按要求填写如表:
| 实验方法 | 观察到的现象 | 结论 |
| 取少量反应后的溶液M于试管中,再加入(填序号)B或C. | 有气泡逸出 | 则溶液M呈酸性. |
分析 (1)根据已有的知识进行分析,二氧化碳容易与氢氧化钠反应生成碳酸钠,进行物质除杂时,选择的除杂试剂不能与原有的物质反应,且与杂质反应时不能生成新的杂质;
(2)酚酞在酸性和中性溶液中为无色,盐酸能与碳酸氢钠反应生成二氧化碳,能与活泼金属反应生成氢气;
(3)根据盐酸与氧化铜反应进行分析.
解答 解:(1)氢氧化钠能与二氧化碳反应生成碳酸钠而变质,应该密封保存,进行物质除杂时,选择的除杂试剂不能与原有的物质反应,且与杂质反应时不能生成新的杂质;为了除去稀氢氧化钠溶液中变质产生的碳酸钠,应该选择氢氧化钙溶液,故填:CO2+2NaOH═Na2CO3+H2O,密封,A;
(2)酚酞溶液不变色,则溶液可能是酸性也可能是中性,盐酸能与碳酸氢钠反应生成二氧化碳,能与活泼金属反应生成氢气,故填:错误;盐酸过量,溶液显酸性;B或C;酸;
(3)盐酸与氧化铜反应,生成氯化铜和水,氧化铜为黑色粉末,氯化铜溶液显蓝色,所以在乙组同学反应后的溶液中加入CuO,反应的实验现象为黑色粉末逐渐消失,溶液由无色变为蓝色;故填:黑色粉末逐渐消失,溶液由无色变为蓝色;
故答案为:(1)CO2+2NaOH═Na2CO3+H2O,密封,A;
(2)错误;盐酸过量,溶液显酸性,酚酞溶液也不变色;B或C;酸
(3)黑色粉末逐渐消失,溶液由无色变为蓝色
点评 本题考查了酸碱中和反应以及物质的性质,完成此题,可以依据已有的知识进行,要求同学们加强对基础知识的储备,以便灵活应用.

练习册系列答案
相关题目
20.下列有关课外实验的说法不正确的是( )
| A. | 加入熟石灰并研磨,可区分氯化铵和硫酸钠 | |
| B. | 在靠近蜡烛火焰的上方放一只冷碟子,一段时间后可收集到炭黑 | |
| C. | 用灼烧并闻气味的方法,可区分羊毛纤维和棉纤维 | |
| D. | 在制作叶脉书签时,一般选用10%的氯化钠溶液 |
17.如图是某化学反应的微观模型,“ ”、“
”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )

 ”、“
”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
| A. | 反应中共有两种元素参与 | |
| B. | 反应物和生成物中只有一种单质 | |
| C. | 该反应属于分解反应 | |
| D. | 参加反应的两种物质分子个数之比为2:3 |
4.如表中对部分化学知识归纳总结正确的是( )
| A | B |
| ①活性炭可以使硬水软化 ②合理施用农药、化肥可减少水体污染 ③点燃可燃性气体前必须验纯 | ①墙内开花墙外香,说明分子在不断运动着 ②酒精溶液是混合物,说明是由不同种分子构成的 ③物质能由分子原子、离子构成 |
| C | D |
| ①用灼烧,闻气味的方法区分棉线和羊毛线 ②用观察颜色的方法区别白酒和白醋 ③用无色酚酞溶液可鉴别稀盐酸和氢氧化钠溶液 | ①热水瓶中的水垢可用食醋除去 ②高炉炼铁是利用一氧化碳的还原性 ③人体中含量较多的前四种元素是氧、碳、氢、氮 |
| A. | A | B. | B | C. | C | D. | D |
14.某同学欲选用下列几组试剂探究 Al、Fe、Cu 三种金属的活动性顺序,其中不能达到目的是( )
| A. | Fe、Cu、Al2(SO4)3溶液 | B. | Al、Cu、FeSO4 溶液 | ||
| C. | Fe、Al2(SO4)3 溶液、CuSO4 溶液 | D. | Al、Fe、Cu、稀 H2SO4 |
18.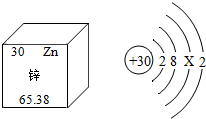 锌是人体必需的微量元素,如图是锌元素的部分信息,下列说法中正确的是( )
锌是人体必需的微量元素,如图是锌元素的部分信息,下列说法中正确的是( )
 锌是人体必需的微量元素,如图是锌元素的部分信息,下列说法中正确的是( )
锌是人体必需的微量元素,如图是锌元素的部分信息,下列说法中正确的是( )| A. | 属于非金属元素 | B. | 原子核外电子数为30 | ||
| C. | 相对原子质量为65.38g | D. | 锌原子结构示意图中X为8 |
19.为验证下列化学变化的发生,需要滴加指示剂才能观察到实验现象的是( )
| A. | 向石灰石中滴加盐酸 | B. | 向氧化铁中滴加硫酸 | ||
| C. | 向水中通入二氧化碳 | D. | 向氢氧化钙溶液中通入二氧化碳 |