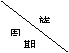
25.(09年广东理基·35)下表是元素周期表的一部分,有关说法正确的是
 |
IA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
2 |
|
|
|
c |
|
d |
|
|
3 |
a |
b |
|
|
|
e |
f |
A.e的氢化物比d的氢化物稳定
B.a、b、e三种元素的原子半径:e>b>a
C.六种元素中,c元素单质的化学性质最活泼
D.c、e、f的最高价氧化物对应的水化物的酸性依次增强
答案:D
解析:根据同周期和同主族性质的递变规律可以判断各选项的正误。A选项e、d元素同主族,且d在第二周期,而e在第三周期,因此d的氢化物比e的氢化物稳定。B选项中a、b、e三种元素同周期,所以其原子半径为a>b>e。这六中元素的单质中c的单质碳石化学性质最不活泼的。
 .(09年海南化学·10)门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是:
.(09年海南化学·10)门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是: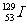 与
与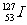 互为同位素
互为同位素

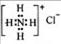

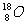
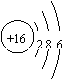
 ,
,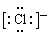 。
。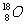 表示质量数为18,质子数为8的氧原子,所以该原子核内有10个中子。
表示质量数为18,质子数为8的氧原子,所以该原子核内有10个中子。
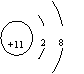

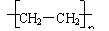
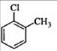
 ,CH2=CH2
,CH2=CH2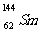 与
与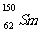 的说法正确的是
的说法正确的是