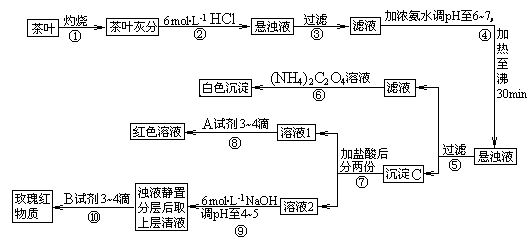
14.[江苏省南通中学2008学年度第一学期期末复习高三化学 ]某中学化学教材上有如下介绍:“在氢氧化钠浓溶液中加入氧化钙,加热,制得白色固体就是碱石灰,它是水和二氧化碳的吸收剂”。有两个实验小组决定通过实验来探究碱石灰的组成。
(1)第一小组设计的实验方案如下:
 w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
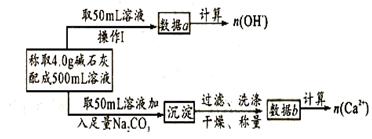
下列关于溶液中n(OH-)、n(Ca2+)、n(Na+)之间的关系式正确的是________
A. n(Na+)+ 2n(Ca2+)= n(OH-) B. 2n(Na+) + 2n(Ca2+)= n(OH-)
C. n(Na+)+ n(Ca2+)= 2n(OH-)
现有4.0g碱石灰,设其中n(Na+)= xmol, n(Ca2+)= ymol,请填写下列空格:
|
碱石灰的可能组成 |
NaOH, CaO |
NaOH,
CaO, Ca(OH)2 |
NaOH, Ca(OH)2 |
NaOH,
Ca(OH)2 H2O |
|
x,y之间关系式(等式或不等式) |
A |
40x+56y﹤4.0﹤ 40x+74y |
B |
C |
把表中A、C的关系式填在下面空格上:
A:__________________________C:______________________ 。
(2)第二小组查得如下资料:氢氧化钙在250℃时不分解,高于250℃时才分解;氢氧化钠在580℃时不分解。他们设计了如下方案并得出相应相关数据:取市售碱石灰4.0g,在250℃时加热至恒重,测得固体质量减少了0.6g,剩余固体在580℃时继续加热至恒重,测得固体质量又减少了0.7g.请通过计算确定该碱石灰各成分的质量分数?(要计算过程)
答案.(1)(3分)A A:40x+56y=4.0 C:40x+74y﹤4.0
(2) (3分)NaOH%=13% Ca(OH)2%=72% H2O%=15%
10.[江苏省前黄高级中学09届上学期高三化学第二次周练卷 ](12分)蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如下:
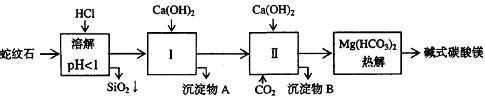
(1) 蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是________。
(2) 进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见下表)Ca(OH)2不能过量, w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
若Ca(OH)2过量可能会导致 溶解、 沉淀。
|
氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
|
开始沉淀pH |
1.5 |
3.3 |
9.4 |
(3) 从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入_________ (填入物质的化学式),然后__________________________________ (依次填写实验操作名称)。
(4) 物质循环使用,能节约资源。上述实验中,可以循环使用的物质是______________(填写物质化学式)。
(5) 现设计一个实验,确定产品aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):①样品称量 ②高温分解 ③______________________________
④_____________________________ ⑤MgO称量
(6) 18.2g产品完全分解后,产生6.6gCO2和8.0g MgO,由此可知,产品的化学式中:
a=_________、b=_________、c=_________。
答案.、(12分)(1)Fe3+ Al3+;(2)Al(OH) 3、Mg(OH)2;(3)NaOH,过滤、洗涤、灼烧;
(4)CO2;(5)③测出CO2的质量;④测出水蒸汽的质量;(6)3、1、3。
7.[江苏省前黄高级中学国际分校09届第一学期期末综合练习二]X、Y、Z、W有如右图所示的转化关系,则X、W可能是 [A]
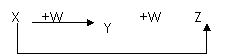 ①C、O2 ②AlCl3、NaOH
①C、O2 ②AlCl3、NaOH
 ③Fe、HNO3 ④S、O2
③Fe、HNO3 ④S、O2
A.①②③ B.①②
C.③④ D.①②③④
8[江苏省前黄高级中学国际分校09届第一学期期末综合练习二].下述实验能达到预期目的的是 [B]
|
编号 |
实验内容 |
实验目的 |
|
A |
金属钠投入硫酸铜溶液中 |
置换出铜 |
|
B |
向硫酸铝溶液中滴加过量氨水 |
制取氢氧化铝 |
|
C |
将氯化铁溶液加热蒸发 |
制氯化铁晶体 |
|
D |
把铜和银用导线连接后插入稀硫酸中 |
组成原电池验证铜比银活泼 |
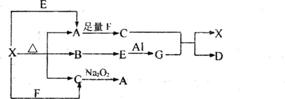
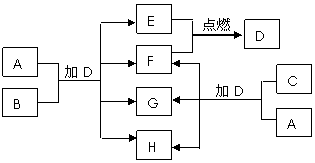 答案..(1)X:NaHC03 G:NaAIO2 D:Al(OH)3
答案..(1)X:NaHC03 G:NaAIO2 D:Al(OH)3 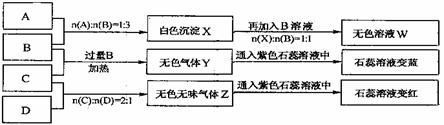
 HCO3-+OH-
HCO3-+OH-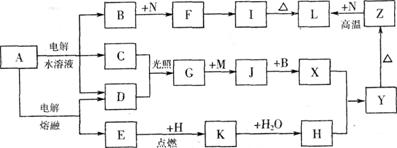
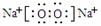
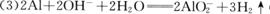 (2分);
(2分);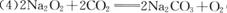 (2分);
(2分);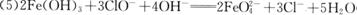 (2分);
(2分);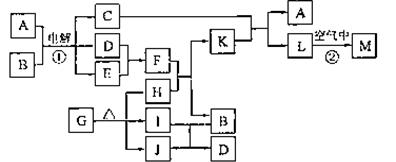
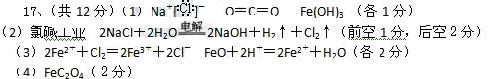
 K2CO3+CO2↑+H2O
K2CO3+CO2↑+H2O  CH3OH(g)+H2O(g) ΔH=-49.47kJ/mol
CH3OH(g)+H2O(g) ΔH=-49.47kJ/mol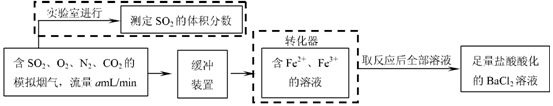 w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m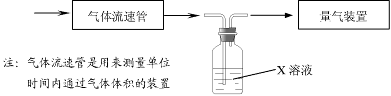
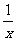 Sx 、
Sx 、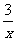 Sx 。其中COS中“C”化合价为
▲ 。
Sx 。其中COS中“C”化合价为
▲ 。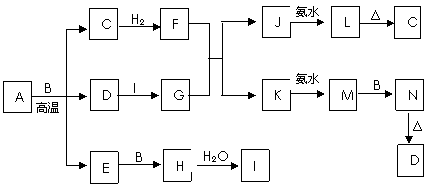 ⑴组成E的两种元素位于同一主族,该两种元素气态氢化物的沸点较高的是(填分子式)
⑴组成E的两种元素位于同一主族,该两种元素气态氢化物的沸点较高的是(填分子式)