摘要:21.近年来有人提出了利用海水处理含二氧化硫的废气.该方法的流程如下:
网址:http://m.1010jiajiao.com/timu_id_919335[举报]
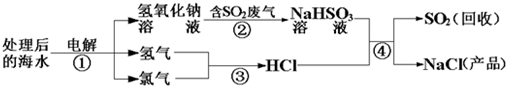
近年来有人提出了利用海水(含氯化钠)处理含二氧化硫的废气,该方法的流程如下图所示.下列说法正确的是( )


| A、可循环利用的物质是SO2 | B、图中反应①属于分解反应 | C、反应中硫元素的化合价发生变化 | D、从海水中最终得到“NaCl(产品)”的过程是物理变化 |
近年来有人提出了利用海水(含氯化钠)处理含二氧化硫的废气,该方法的流程如下:
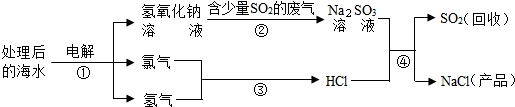
(1)图中从海水最终得到“NaCl(产品)”的过程属于 (填“物理变化”或“化学变化”).
(2)①中的反应物是氯化钠和 ,该反应的化学方程式为 .
(3)图中反应①、③、④属于化合反应的是 (填序号).
(4)反应④的化学方程式为 .
查看习题详情和答案>>

(1)图中从海水最终得到“NaCl(产品)”的过程属于
(2)①中的反应物是氯化钠和
(3)图中反应①、③、④属于化合反应的是
(4)反应④的化学方程式为
近年来有人提出了利用海水(含氯化钠)处理含二氧化硫的废气,该方法的流程如下:
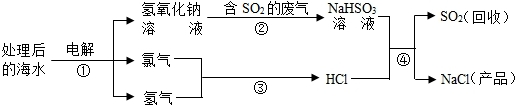
(1)上图中从海水最终得到“NaCl(产品)”的过程属于 (填“物理变化”或“化学变化”).
(2)图中反应①、③、④属于化合反应的是 (填序号).
(3)①中的反应物是氯化钠和 ,该反应的化学方程式为 .
(4)反应④的化学方程式为 .
查看习题详情和答案>>

(1)上图中从海水最终得到“NaCl(产品)”的过程属于
(2)图中反应①、③、④属于化合反应的是
(3)①中的反应物是氯化钠和
(4)反应④的化学方程式为
近年来有人提出了利用海水(含氯化钠)处理含二氧化硫的废气,该方法的工艺流程如图所示.

(1).写出①反应的化学方程式:
(2)反应前后硫元素的化合价
(3)从海水中最终得到“NaCl(溶液)”的过程是
查看习题详情和答案>>

(1).写出①反应的化学方程式:
2NaCl+2H2O
2NaOH+Cl2↑+H2↑
| ||
2NaCl+2H2O
2NaOH+Cl2↑+H2↑
反应的类型是
| ||
不属于化合、分解、置换和复分解反应
不属于化合、分解、置换和复分解反应
.(2)反应前后硫元素的化合价
否
否
(选“是”或“否”)发生变化(3)从海水中最终得到“NaCl(溶液)”的过程是
化学
化学
变化;要由NaCl(溶液)得到NaCl(晶体)还要经过蒸发
蒸发
过程.利用1000g15% NaCl溶液来选种,需产品25%NaCl溶液600
600
g,水400
400
g来配制.