摘要:15.取两枚质量相等的铁钉.第一枚密封保存.第二枚露置于空气中致其部分生锈.然后将这两枚铁钉分别与足量的稀盐酸完全反应.其结果是 A.第二枚铁钉反应后消耗的盐酸多 B.两者消耗的盐酸一样多 C.第一枚铁钉反应后消耗的盐酸多 D.二者产生的氢气一样多
网址:http://m.1010jiajiao.com/timu_id_918630[举报]
现有以下常见化学实验装置,请按要求回答问题:
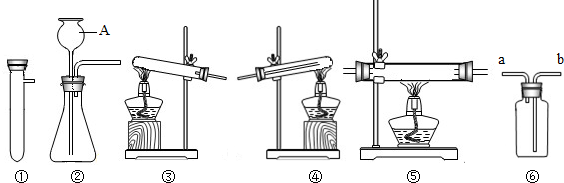
(1)仪器A的名称为 ;可用作洗涤或干燥气体的装置是 (填序号).
(2)可用作实验室制取CO2和用双氧水制取氧气发生装置的是 (填序号),其中实验室制取CO2的化学方程式为 .用装置③制取氧气的化学方程式是 .
(3)实验室制取氢气用的是粗锌和稀硫酸.用稀硫酸而不用盐酸的原因是 ;用粗锌比用纯锌反应速率更快,这是因为粗锌中含可溶性的杂质或能与酸反应的杂质,这些杂质的存在可大大提高该反应的速率.取两份质量相等的纯锌粉,编号为a和b,在b中加入少量的氧化铜粉末,将a和b分别投入足量的稀硫酸中,充分反应后,则:
产生氢气的质量:a b(填>﹦<,下同);产生氢气的速率:a b.
查看习题详情和答案>>

(1)仪器A的名称为
(2)可用作实验室制取CO2和用双氧水制取氧气发生装置的是
(3)实验室制取氢气用的是粗锌和稀硫酸.用稀硫酸而不用盐酸的原因是
产生氢气的质量:a
(2010?武清区二模)
今年春晚刘谦表演的近景魔术如真似幻,让人大饱眼福,陈老师也在化学晚会上表演如下魔术:用毛笔蘸取一种无色液体在一张白纸上书写了“中考必胜”四字,然后再喷上一种无色液体,白纸上立即出现了红色的“中考必胜”四字.你能揭底陈老师他先后所用的无色液体可能是
A.石蕊溶液、NaOH溶液 B.酚酞溶液、“雪碧”饮料
C.澄清石灰水、酚酞溶液 D.Fe2(SO4)3溶液、NaOH溶液
碳酸钠俗称纯碱,其溶液能使无色酚酞变红,甲同学想探究是Na+还是CO32-的作用使酚酞试液变红,其设计方案如下:先往Na2CO3溶液中滴加酚酞试液后,再加入适量的Ca(OH)2溶液,观察红色是否消失.资料查询:纯碱是一种盐,其溶液pH>7,氯化钙溶液pH=7.
①老师肯定了乙同学的看法,你认为甲同学方案的不合理之处是
②丙同学要证明是CO32-的作用使酚酞试液变红.在下列物质中选用一种最好的试剂是(填序号)
③丁同学发现碳酸钠溶液碱性的强弱与溶液的浓度和温度有关,请你帮他完成实验探究.(只要求就一种影响碳酸钠溶液碱性强弱的因素设计实验方案.)
[实验方案]
查看习题详情和答案>>

今年春晚刘谦表演的近景魔术如真似幻,让人大饱眼福,陈老师也在化学晚会上表演如下魔术:用毛笔蘸取一种无色液体在一张白纸上书写了“中考必胜”四字,然后再喷上一种无色液体,白纸上立即出现了红色的“中考必胜”四字.你能揭底陈老师他先后所用的无色液体可能是
C
C
A.石蕊溶液、NaOH溶液 B.酚酞溶液、“雪碧”饮料
C.澄清石灰水、酚酞溶液 D.Fe2(SO4)3溶液、NaOH溶液
碳酸钠俗称纯碱,其溶液能使无色酚酞变红,甲同学想探究是Na+还是CO32-的作用使酚酞试液变红,其设计方案如下:先往Na2CO3溶液中滴加酚酞试液后,再加入适量的Ca(OH)2溶液,观察红色是否消失.资料查询:纯碱是一种盐,其溶液pH>7,氯化钙溶液pH=7.
①老师肯定了乙同学的看法,你认为甲同学方案的不合理之处是
Ca(OH)2溶液与Na2CO3溶液反应后的产物中含有能使无色酚酞试液变红的NaOH,干扰实验
Ca(OH)2溶液与Na2CO3溶液反应后的产物中含有能使无色酚酞试液变红的NaOH,干扰实验
;②丙同学要证明是CO32-的作用使酚酞试液变红.在下列物质中选用一种最好的试剂是(填序号)
C
C
;A.HCl B.NaOH C.CaCl2③丁同学发现碳酸钠溶液碱性的强弱与溶液的浓度和温度有关,请你帮他完成实验探究.(只要求就一种影响碳酸钠溶液碱性强弱的因素设计实验方案.)
[实验方案]
在相同的温度下,取两份质量相等浓度不同Na2CO3溶液,分别用pH试纸测出其pH值进行比较,多测几次再下结论.或取两份质量相等的同种Na2CO3溶液,分别用pH试纸测出其在不同温度时pH值进行比较,多测几次再下结论
在相同的温度下,取两份质量相等浓度不同Na2CO3溶液,分别用pH试纸测出其pH值进行比较,多测几次再下结论.或取两份质量相等的同种Na2CO3溶液,分别用pH试纸测出其在不同温度时pH值进行比较,多测几次再下结论
.29、(1)化学小组同学用下列仪器和试剂,验证金属与盐酸反应速率的影响因素.
实验仪器:烧杯、石棉网、酒精灯、铁架台(带铁圈)、镊子、量筒、天平等.
实验试剂:锌片、铁片、镁片.溶质质量分数分别为5%、20%的盐酸.
①不同金属与酸反应的快慢不同取质量相等的镁、锌、铁中两种金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图所示.则线B对应的金属为

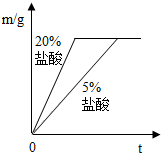
②同种金属与不同溶质质量分数的盐酸反应的快慢不同取两份质量相等的锌片,分别放入5%和20%的足量
稀盐酸中,生成氢气的质量为m,反应时间为t.对比5%和20%的稀盐酸分别与锌片反应情况,下列关系曲线正确的是
A. B.
B. C.
C. D.
D.
实验表明,盐酸中溶质的质量分数越大,与金属反应的速率越快.
③温度对金属与盐酸反应速率也有影响,且实验表明,温度越高,盐酸与金属反应的速率越快.请用控制变量的方法设计实验,验证以上结论,实验方案为
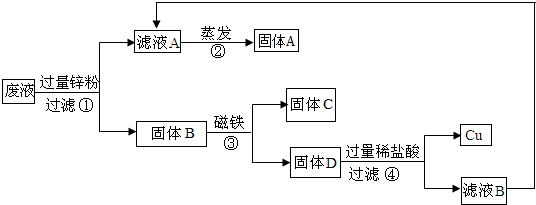
(2)同学们做完实验后,将含有CuCl2、ZnCl2、FeCl2的废液倒在废液缸里,如果将废液直接排放,就会造成水污染.于是几位同学利用课余时间处理废液,回收工业重要原料氯化锌和有关金属.实验过程如下图所示.

请回答:
①滤液A和滤液B含有的一种相同溶质的化学式是
②写出步骤①反应的化学方程式
③检验步骤④中加入的稀盐酸是否过量的方法是
查看习题详情和答案>>
实验仪器:烧杯、石棉网、酒精灯、铁架台(带铁圈)、镊子、量筒、天平等.
实验试剂:锌片、铁片、镁片.溶质质量分数分别为5%、20%的盐酸.
①不同金属与酸反应的快慢不同取质量相等的镁、锌、铁中两种金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图所示.则线B对应的金属为
Zn
,线A对应的金属与稀盐酸反应的化学方程式为
Fe+2HCl═FeCl2+H2↑
.
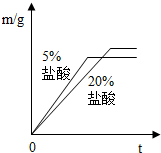
②同种金属与不同溶质质量分数的盐酸反应的快慢不同取两份质量相等的锌片,分别放入5%和20%的足量
稀盐酸中,生成氢气的质量为m,反应时间为t.对比5%和20%的稀盐酸分别与锌片反应情况,下列关系曲线正确的是
C
(填字母序号).A.
 B.
B. C.
C. D.
D.
实验表明,盐酸中溶质的质量分数越大,与金属反应的速率越快.
③温度对金属与盐酸反应速率也有影响,且实验表明,温度越高,盐酸与金属反应的速率越快.请用控制变量的方法设计实验,验证以上结论,实验方案为
取两份质量相等的铁片,分别放入盛有5%的足量稀盐酸的烧杯中,将其中一只烧杯里溶液加热,观察两只烧杯中产生气泡的快慢
.(2)同学们做完实验后,将含有CuCl2、ZnCl2、FeCl2的废液倒在废液缸里,如果将废液直接排放,就会造成水污染.于是几位同学利用课余时间处理废液,回收工业重要原料氯化锌和有关金属.实验过程如下图所示.

请回答:
①滤液A和滤液B含有的一种相同溶质的化学式是
ZnCl2
;②写出步骤①反应的化学方程式
Zn+CuCl2═ZnCl2+Cu
;③检验步骤④中加入的稀盐酸是否过量的方法是
Zn+FeCl2═Fe+ZnCl2
.
 B.
B.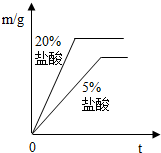
 D.
D.