摘要:“谈奶色变 的主角三聚氰胺的结构简式为(1)下列关于三聚氰胺的说法中正确的是 A.属于芳香烃的衍生物 B.属于高分子化合物C.属于氨基酸 D.可与多种酸反应生成盐(2)目前较多采用尿素[CO(NH2)2]法合成三聚氰胺.即在催化剂和380~400℃条件下反应生成三聚氰胺.同时还得到酸碱性刚好相反的两种气体.试写出该反应的化学方程式: ,(3)已知三聚氰胺遇强酸或强碱的水溶液能水解生成三聚氰酸[C3N3(OH)3.其中N呈―3价].三聚氰酸在加热条件下可用于消除汽车尾气中的NO2.其反应原理为 .(4)某品牌奶粉中蛋白质含量为18%.若蛋白质中平均含氮量为16%.则该奶粉的含氮量为 .若向1袋(400g)该品牌奶粉中加入1g三聚氰胺.则从含氮量看.相当与增加了 g蛋白质.白鹭洲中学2008―2009年高二(下)期中化学考试试卷答题卡12345678910111213141516
网址:http://m.1010jiajiao.com/timu_id_91666[举报]
日本核泄漏中最危险的是131I,较大量接触对人体有害,所以不必“谈碘色变”。131 53I在人类生活中还有着“天使”的一面,如控制剂量在医疗上有助于治疗多种甲状腺疾病。在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘。
已知:步骤③中发生的反应是:Fe+2AgI=FeI2+2Ag。
莫尔盐的化学式为:(NH4)2Fe (SO4)2·6H2O。
已知:步骤③中发生的反应是:Fe+2AgI=FeI2+2Ag。
莫尔盐的化学式为:(NH4)2Fe (SO4)2·6H2O。

⑴鉴别丙、丁溶液中的金属阳离子可选用的试剂是___________溶液。
⑵步骤④中加入稀H2SO4浸洗的目的是______________。
⑶上述生产流程中,可以循环利用的物质是____________。
⑷“⑦系列操作”包含的操作名称依次为蒸发浓缩、__________、___________、洗涤、干燥。
⑸为了测定富碘卤水中碘离子的含量,可用高锰酸钾滴定法。已知高锰酸钾和碘离子的反应为:2MnO4-+10I-+16H+=2Mn2++5I2+8H2O。
填空:
① 取20.00mL富碘卤水放入__________(填仪器名称)中,将0.1 mol·L-1的酸性高锰酸钾溶液装入滴定管中,达到滴定终点的标志是________________。
② 三次滴定消耗高锰酸钾溶液的部分数据如下表,
⑵步骤④中加入稀H2SO4浸洗的目的是______________。
⑶上述生产流程中,可以循环利用的物质是____________。
⑷“⑦系列操作”包含的操作名称依次为蒸发浓缩、__________、___________、洗涤、干燥。
⑸为了测定富碘卤水中碘离子的含量,可用高锰酸钾滴定法。已知高锰酸钾和碘离子的反应为:2MnO4-+10I-+16H+=2Mn2++5I2+8H2O。
填空:
① 取20.00mL富碘卤水放入__________(填仪器名称)中,将0.1 mol·L-1的酸性高锰酸钾溶液装入滴定管中,达到滴定终点的标志是________________。
② 三次滴定消耗高锰酸钾溶液的部分数据如下表,

则V3=_____________mL,请根据数据计算富碘卤水中c(I-)=_____________mol·L-1。(精确到0.01)
查看习题详情和答案>>
(2011?崇明县二模)53131I是日本核泄漏的元素之一,较大量接触对人体有害,所以不必“谈碘色变”.53131I在人类生活中还有着“天使”的一面,如控制剂量在医疗上有助于治疗多种甲状腺疾病.下面对53131I的叙述中错误的是( )
查看习题详情和答案>>
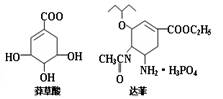
 2005年禽流感在全球蔓延,百姓谈“禽”色变.目前通过从香料八角中提取的莽草酸制得的达菲是抗禽流感病毒特效药物.下列有关描述正确的是( )
2005年禽流感在全球蔓延,百姓谈“禽”色变.目前通过从香料八角中提取的莽草酸制得的达菲是抗禽流感病毒特效药物.下列有关描述正确的是( )