摘要:5100116氯化镁
网址:http://m.1010jiajiao.com/timu_id_914045[举报]
(2011?鼓楼区二模)某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品.
(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和氯化镁.上述几种物质在不同温度时的溶解度数据如下表:
根据所提供的溶解度数据,画出硫酸钠的溶解度曲线.
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下:

(1)“降温”的目的是析出副产品“A晶体”,它是______ (写对应溶质的化学式)析出的晶体.
(2)“盐水精制I”中发生反应的化学方程式是______.
(3)“盐水精制Ⅱ中发生反应的化学方程式是______.
(4)经过上述精制过程中,仍有一种物质并没有能够完全除去,该物质可以在溶液精制过程中步骤______(填序号)后加入稍过量的______溶液除去.
(三)用上述精制后的食盐水为原料生产的纯碱产品中会含有少量氯化钠杂质.该制碱厂的
产品包装袋上注明:碳酸钠含量≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取18.0g纯碱样晶放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.Og,再把lOOg稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
 查看习题详情和答案>>
查看习题详情和答案>>
(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和氯化镁.上述几种物质在不同温度时的溶解度数据如下表:
| 温度/℃ | 10 | 20 | 30 | 40 | ||
| 溶 | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 解 | 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 |
| 度 | 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 |
| /g | 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 |
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下:

(1)“降温”的目的是析出副产品“A晶体”,它是______ (写对应溶质的化学式)析出的晶体.
(2)“盐水精制I”中发生反应的化学方程式是______.
(3)“盐水精制Ⅱ中发生反应的化学方程式是______.
(4)经过上述精制过程中,仍有一种物质并没有能够完全除去,该物质可以在溶液精制过程中步骤______(填序号)后加入稍过量的______溶液除去.
(三)用上述精制后的食盐水为原料生产的纯碱产品中会含有少量氯化钠杂质.该制碱厂的
产品包装袋上注明:碳酸钠含量≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取18.0g纯碱样晶放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.Og,再把lOOg稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 盐酸的质量 | 25 | 25 | 25 | 25 |
| 烧杯及所盛物质总质量 | 180.3 | 202.6 | 226.4 | 251.4 |
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______g.
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
 查看习题详情和答案>>
查看习题详情和答案>>
某盐水主要是含氯化钠,此外还含有较多硫酸钠,以及少量的氯化钙和氯化镁.
上述几种物质在不同温度时的溶解度数据如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 |
(2)根据所提供的溶解度数据,画出氯化镁的溶解度曲线;

(3)从溶液中获得硫酸钠晶体适宜采用________的方法.
(4)30℃时,100g氯化钙饱和溶液中,氯化钙的质量为________g. 查看习题详情和答案>>
某盐水主要是含氯化钠,此外还含有较多硫酸钠,以及少量的氯化钙和氯化镁.
上述几种物质在不同温度时的溶解度数据如下表:
(1)在同温下,溶解度最大的物质是______.
(2)根据所提供的溶解度数据,画出氯化镁的溶解度曲线;

(3)从溶液中获得硫酸钠晶体适宜采用______的方法.
(4)30℃时,100g氯化钙饱和溶液中,氯化钙的质量为______g.
查看习题详情和答案>>
上述几种物质在不同温度时的溶解度数据如下表:
| 温度/℃ | 10 | 20 | 30 | 40 | ||
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 |
(2)根据所提供的溶解度数据,画出氯化镁的溶解度曲线;

(3)从溶液中获得硫酸钠晶体适宜采用______的方法.
(4)30℃时,100g氯化钙饱和溶液中,氯化钙的质量为______g.
查看习题详情和答案>>
某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品.
(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和氯化镁.上述几种物质在不同温度时的溶解度数据如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |
(2)10℃时由100g水配制得到的饱和硫酸钠溶液中溶质的质量是______g,溶质的质量分数是______(精确到0.1%).
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下:
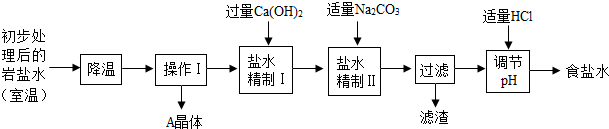
(3)“降温”的目的是析出副产品“A晶体”,A的化学式是______.
(4)“操作I”中的操作是______,若在实验室进行该操作,需要用到的玻璃仪器除烧杯、玻璃棒外,还有______.
(5)“盐水精制I”是除去盐水中的少量氯化镁,反应的化学方程式是______.
(6)“盐水精制Ⅱ”是除去盐水中的其他杂质,反应的化学方程式是______. 查看习题详情和答案>>
(2008?广州)某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品.
(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和氯化镁.上述几种物质在不同温度时的溶解度数据如下表:
(1)根据所提供的溶解度数据,画出硫酸钠的溶解度曲线.
(2)10℃时由100g水配制得到的饱和硫酸钠溶液中溶质的质量是g,溶质的质量分数是(精确到0.1%).
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下:
(3)“降温”的目的是析出副产品“A晶体”,A的化学式是.
(4)“操作I”中的操作是,若在实验室进行该操作,需要用到的玻璃仪器除烧杯、玻璃棒外,还有.
(5)“盐水精制I”是除去盐水中的少量氯化镁,反应的化学方程式是.
(6)“盐水精制Ⅱ”是除去盐水中的其他杂质,反应的化学方程式是. 查看习题详情和答案>>
(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和氯化镁.上述几种物质在不同温度时的溶解度数据如下表:
| 温度/℃ | 10 | 20 | 30 | 40 | ||
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |
(2)10℃时由100g水配制得到的饱和硫酸钠溶液中溶质的质量是g,溶质的质量分数是(精确到0.1%).
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下:

(3)“降温”的目的是析出副产品“A晶体”,A的化学式是.
(4)“操作I”中的操作是,若在实验室进行该操作,需要用到的玻璃仪器除烧杯、玻璃棒外,还有.
(5)“盐水精制I”是除去盐水中的少量氯化镁,反应的化学方程式是.
(6)“盐水精制Ⅱ”是除去盐水中的其他杂质,反应的化学方程式是. 查看习题详情和答案>>