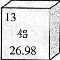
摘要:A.铝的元素符号是Ag B.铝的原子序数是26.98 C.铝的核内质子数是13 D.铝在反应中易得到电子
网址:http://m.1010jiajiao.com/timu_id_913393[举报]
(2007
,安徽,6)元素周期表中铝元素的部分信息如图所示,下列说法正确的是[
]
|
A .铝的元素符号是Ag |
B .铝的原子序数是26.98 |
|
C .铝的核内质子数是13 |
D .铝在反应中易得到电子 |
 金属是一类重要的材料,人类的生活和生产都离不开金属.
金属是一类重要的材料,人类的生活和生产都离不开金属.(1)小琴同学设计如图所示的A、B两个实验.
①在做A,B实验之前,她进行的操作是
用砂纸将铁丝和银丝表面打磨光亮
用砂纸将铁丝和银丝表面打磨光亮
;②做A实验时,将铁丝和银丝同时插入稀硫酸中所发生反应的化学方程式
Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
,其实验目的是比较铁和银的金属活动性强弱
比较铁和银的金属活动性强弱
;③B实验中,当烧杯内盛有
CuSO4
CuSO4
溶液时,可验证Fe、Cu
Cu
、Ag三种金属活动性强弱.(2)钛合金是21世纪的重要材料,具有熔点高、可塑性好、抗腐蚀性强、与人体有很好的“相容性”等优良性能.金属的下列用途:①用来做保险丝 ②用来制人造骨 ③用于制造船舶 ④用于制造航天飞机.其中与钛合金性能符合的是
②③④
②③④
(填序号).(3)常见的三种金属被发现、使用的先后顺序依次为:铜、铁、铝.金属大规模被使用的先后顺序跟下列
③
③
(填序号)选项关系最大.①地壳中金属元素的含量 ②金属的导电性 ③金属活动性(4)颗粒达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”.实验室制备的方法是:以高纯氮气作保护气,在高温条件下用H2和FeCl2发生置换反应,生成“纳米铁”,其化学方程式为
FeCl2+H2
Fe+2HCl
| ||
FeCl2+H2
Fe+2HCl
,反应中需要保护气的原因是
| ||
防止铁在高温下与氧气反应
防止铁在高温下与氧气反应
.31、整理和归纳、探究是有效的学习方法.下面是恭城县民族中学化学学习小组的同学对Mg、Al、Fe、Mn、Cu、Hg、Ag五种金属相关知识的归纳复习,请你参与并回答问题:
(1)从物理性质上看,每种金属都有自己的特性.你认为汞与其它金属的不同之处是
(2)性质决定用途,用途反映性质是重要的化学学科思想.用镁粉制作的烟花在夜空中发出耀眼的白光,这是利用了镁的
(3)铝的化学性质比铁要活泼,但是铝制品却很耐腐蚀,其原因是
(4)该化学兴趣小组的同学为了探究铁(Fe)、锰(Mn)和铜(Cu)三种金属的活动性顺序,进行下列探究.
①同学们将等大小的三种金属同时放入等质量、等质量分数的稀硫酸中,发现锰表面冒出气泡的速率比铁快,而铜表面无现象.请将三种金属的元素符号填入下表:
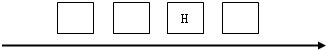
如果金属锰与稀硫酸反应生成的盐是硫酸锰(MnSO4),请你写出锰与稀硫酸反应的化学方程式
②兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液.他们想从中回收金属铜和硫酸亚铁晶体,设计了如下方案:
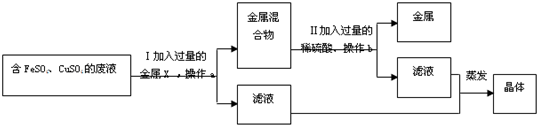
①甲同学提出X可用金属铁,乙同学认为X可用金属锰,你认为
②操作a、b的名称是
查看习题详情和答案>>
(1)从物理性质上看,每种金属都有自己的特性.你认为汞与其它金属的不同之处是
常温下Hg是液体而其余均为固体.
.(2)性质决定用途,用途反映性质是重要的化学学科思想.用镁粉制作的烟花在夜空中发出耀眼的白光,这是利用了镁的
可燃
性.(3)铝的化学性质比铁要活泼,但是铝制品却很耐腐蚀,其原因是
铝易与氧气反应生成氧化铝的保护膜
.(4)该化学兴趣小组的同学为了探究铁(Fe)、锰(Mn)和铜(Cu)三种金属的活动性顺序,进行下列探究.
①同学们将等大小的三种金属同时放入等质量、等质量分数的稀硫酸中,发现锰表面冒出气泡的速率比铁快,而铜表面无现象.请将三种金属的元素符号填入下表:

如果金属锰与稀硫酸反应生成的盐是硫酸锰(MnSO4),请你写出锰与稀硫酸反应的化学方程式
Mn+H2SO4=MnSO4+H2↑
.②兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液.他们想从中回收金属铜和硫酸亚铁晶体,设计了如下方案:

①甲同学提出X可用金属铁,乙同学认为X可用金属锰,你认为
甲
(选填“甲”或“乙”)同学的意见是正确的,理由是可得到纯净的FeSO4晶体
.加入过量的金属X的目的是使废液中的铜全部被置换出来
.②操作a、b的名称是
过滤
,其目的是除去溶液中不溶性
的杂质.步骤Ⅱ中发生反应的化学方程式为Fe+H2SO4=FeSO4+H2↑
.