摘要:C.2Al+3CuSO4==Al2(SO4)3+3Cu D.2H2O22H2O+O2↑
网址:http://m.1010jiajiao.com/timu_id_910286[举报]
17、中国2010上海世博会的主题是“城市,让生活更美好”.
(1)上海世博园上空飘浮着“鲸鱼”状巨大的系留气球,全天候为世博会安全保障、电视转播提供服务.为了安全,气球内充入的气体是
(2)世博园内用“活性炭+超滤膜+紫外线”组合工艺获得直饮水.其中活性炭起
(3)世博金条已面世,成为收藏热点.但也有不法商贩利用黄金和黄铜外观相似,来制假世博金条来欺骗消费者,你可以用哪种化学试剂来揭穿?
(4)被誉为“东方之冠”的中国馆是上海世博会标志性建筑之一,中国馆共向地下钻孔约5000根钢筋水泥桩,其横梁、椽子、斜撑、柱子的“中国红”外衣选用的是铝板,馆周围是大片红木色的塑木(塑料和木屑按照近似于1:1的比例制成)地板.
①以上建筑中使用了合成材料的是
A.地下桩 B.地板 C.横梁外衣
②铝与NaOH溶液反应化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3X,X的化学式为
③将铝丝浸入硫酸铜溶液中能形成美丽的“铜树”,发生反应的化学方程式为:
(5)太阳能光伏发电是世博会历史上太阳能发电技术最大规模的应用,总装机容量超过4.68兆瓦.太阳能光伏发电最关键的材料是高纯硅,生产高纯硅的流程示意图如下:

①整个制备过程必须达到无水无氧.在H2还原SiHCl3过程中若混入O2,可能引起的后果是
②为了达到绿色化学和节约资源的目的,物质A需要循环使用,A的化学式是
查看习题详情和答案>>
(1)上海世博园上空飘浮着“鲸鱼”状巨大的系留气球,全天候为世博会安全保障、电视转播提供服务.为了安全,气球内充入的气体是
氦气(或He)
.(2)世博园内用“活性炭+超滤膜+紫外线”组合工艺获得直饮水.其中活性炭起
吸附
作用;用紫外线代替氯气对水进行处理,其作用是消毒
.(3)世博金条已面世,成为收藏热点.但也有不法商贩利用黄金和黄铜外观相似,来制假世博金条来欺骗消费者,你可以用哪种化学试剂来揭穿?
盐酸(或稀硫酸、AgNO3溶液等)
.(4)被誉为“东方之冠”的中国馆是上海世博会标志性建筑之一,中国馆共向地下钻孔约5000根钢筋水泥桩,其横梁、椽子、斜撑、柱子的“中国红”外衣选用的是铝板,馆周围是大片红木色的塑木(塑料和木屑按照近似于1:1的比例制成)地板.
①以上建筑中使用了合成材料的是
B
.A.地下桩 B.地板 C.横梁外衣
②铝与NaOH溶液反应化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3X,X的化学式为
H2
.③将铝丝浸入硫酸铜溶液中能形成美丽的“铜树”,发生反应的化学方程式为:
2Al+3CuSO4═Al2(SO4)3+3Cu
(5)太阳能光伏发电是世博会历史上太阳能发电技术最大规模的应用,总装机容量超过4.68兆瓦.太阳能光伏发电最关键的材料是高纯硅,生产高纯硅的流程示意图如下:

①整个制备过程必须达到无水无氧.在H2还原SiHCl3过程中若混入O2,可能引起的后果是
硅被氧化得不到高纯硅,同时可能爆炸
;②为了达到绿色化学和节约资源的目的,物质A需要循环使用,A的化学式是
HCl
. 19、被誉为“东方之冠”的中国馆是上海世博会标志性建筑之一,中国馆共向地下钻孔约5000根钢筋水泥桩,其横梁、椽子、斜撑、柱子的“中国红”外衣选用的是铝板,馆周围是大片红木色的塑木(塑料和木屑按照近似于1:1的比例制成)地板.
19、被誉为“东方之冠”的中国馆是上海世博会标志性建筑之一,中国馆共向地下钻孔约5000根钢筋水泥桩,其横梁、椽子、斜撑、柱子的“中国红”外衣选用的是铝板,馆周围是大片红木色的塑木(塑料和木屑按照近似于1:1的比例制成)地板.(1)以上建筑中使用了合成材料的是
B
.A.地下桩 B.地板 C.横梁外衣
(2)钢和铝的共同点是
C
.A.都是单质 B.都是合金 C.都能导电
(3)铝能与NaOH溶液反应,化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3X,X的化学式为
H2
.(4)将铝丝浸入硫酸铜溶液中能形成美丽的“铜树”,发生反应的化学方程式为:
2Al+3CuSO4=Al2(SO4)3+3Cu
.23、我能根据金属的有关知识进行如下探究实验:
【实验一】
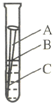
如图,取一根约10cm的光亮铁钉放在自来水中,观察A、B、C三处的变化.几天后,会发现
【实验二】
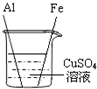
小宁同学用图所示的实验探究Fe、Cu、Al三种金属的活动性顺序.
(1)铝和铁插入溶液前,要除去它们表面的氧化物或污物,方法是
(2)实验时观察到的主要现象是
(3)我认为小宁同学设计的实验不能达到实验目的,原因是
查看习题详情和答案>>
【实验一】

如图,取一根约10cm的光亮铁钉放在自来水中,观察A、B、C三处的变化.几天后,会发现
B
处最先出现铁锈,铁生锈的主要原因是铁与氧气
、水
等物质发生了复杂的化学反应.【实验二】

小宁同学用图所示的实验探究Fe、Cu、Al三种金属的活动性顺序.
(1)铝和铁插入溶液前,要除去它们表面的氧化物或污物,方法是
用砂纸打磨金属表面
.(2)实验时观察到的主要现象是
铝和铁表面都附有红色的物质
,得出的结论是铝和铁比铜的化学性质更活泼
.写出其中一种金属与硫酸铜溶液反应的化学方程式2Al+3CuSO4═Al2(SO4)3+3Cu(或Fe+CuSO4═FeSO4+Cu)
.(3)我认为小宁同学设计的实验不能达到实验目的,原因是
无法比较金属铝与铁的活动性
.因此需另外设计一个实验,才能得出正确的结论.我能设计这个实验并完成下表:| 操 作 | 现 象 | 结 论 |
方法一:把铝线、铁线、铜线同时插入盐酸中. 方法二:把铁线分别插入硫酸铝溶液和硫酸铜溶液中. |
铝表面产生的气泡比铁表面产生的气泡更多更快.铜线表面没有现象. 插入硫酸铝溶液中的铁线表面没现象,插入硫酸铜溶液中的铁表面出现红色的物质. |
三种金属活动性由强到弱的顺序是:Al、Fe、Cu |