摘要:34.进行有关气体的实验.必须先检验装置的 .下述3图中.装置气密性良好的是 .
网址:http://m.1010jiajiao.com/timu_id_906502[举报]
下列有关实验操作的叙述错误的是( )
查看习题详情和答案>>
| A.给玻璃器皿加热时都需垫上石棉网 |
| B.可燃性气体点燃前必须检验其纯度 |
| C.实验产生的废液应倒入指定的容器内 |
| D.实验室制取气体,首先要对装置的气密性进行检查 |
下列有关实验操作的叙述错误的是
- A.给玻璃器皿加热时都需垫上石棉网
- B.可燃性气体点燃前必须检验其纯度
- C.实验产生的废液应倒入指定的容器内
- D.实验室制取气体,首先要对装置的气密性进行检查
4、利用如图所示的实验装置,研究CO的化学性质,回答下列有关问题:
(1)实验时,在加热前必须先通入一段时间的CO,其目的是
(2)CO与灼热的CuO反应生成Cu和CO2,得出该结论所依据的有关实验现象是
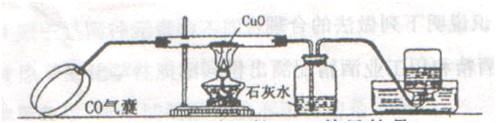
(3)已知草酸(化学式为H2C2O4)受热发生如下反应:H2C2O4=CO↑+CO2↑+H2O,若将该反应生成的气体干燥后收集到如图所示的气囊中进行实验,实验时是否需要对上述装置进行改进,请说明改进的方案和理由:
(4)实验结束后,必须对集气瓶中的气体进行处理,不能让其排放到空气中,原因是
查看习题详情和答案>>
(1)实验时,在加热前必须先通入一段时间的CO,其目的是
防止爆炸
.(2)CO与灼热的CuO反应生成Cu和CO2,得出该结论所依据的有关实验现象是
黑色氧化铜变成红色,石灰水变浑浊
.
(3)已知草酸(化学式为H2C2O4)受热发生如下反应:H2C2O4=CO↑+CO2↑+H2O,若将该反应生成的气体干燥后收集到如图所示的气囊中进行实验,实验时是否需要对上述装置进行改进,请说明改进的方案和理由:
从气囊中排出气体应依次通过氢氧化钠溶液和浓硫酸这样可除尽其中二氧化碳防止对生物二氧化碳检验造成干扰
.(4)实验结束后,必须对集气瓶中的气体进行处理,不能让其排放到空气中,原因是
一氧化碳具有毒性会污染空气
.为探究燃烧的条件,小花同学查阅资料得知:白磷为蜡状固体,有剧毒,不溶于水,着火点为40℃,红磷着火点为240℃.然后她进行了如图实验:
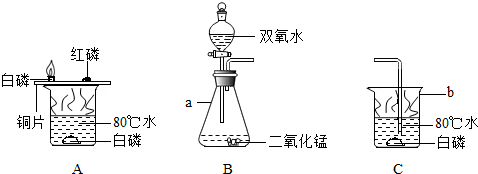
(1)说出图中有关仪器的名称:a
(2)按A装置进行实验,可观察到的现象为:①铜片上的红磷
(3)在使用组装好的B装置前首先应该进行的操作是
(4)从以上实验分析得出,燃烧需要的条件为:
可燃物、
查看习题详情和答案>>

(1)说出图中有关仪器的名称:a
锥形瓶
锥形瓶
、b烧杯
烧杯
.(2)按A装置进行实验,可观察到的现象为:①铜片上的红磷
不燃烧
不燃烧
;②铜片上的白磷燃烧,产生大量白烟
燃烧,产生大量白烟
;③水下的白磷不燃烧
不燃烧
.(3)在使用组装好的B装置前首先应该进行的操作是
检查装置的气密性
检查装置的气密性
,然后加入药品并将B装置和C装置相连接,逐渐滴入双氧水,B装置中反应的化学方程式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
,其中Mn02的作用是
| ||
催化作用
催化作用
,C装置中水下的白磷燃烧.(4)从以上实验分析得出,燃烧需要的条件为:
可燃物、
可燃物必须和氧气(或空气)接触
可燃物必须和氧气(或空气)接触
和温度必须达到可燃物的着火点
温度必须达到可燃物的着火点
.27、做硫在氧气中燃烧的实验时,在集气瓶内放了少量水来吸收SO2,实验结束后,集气瓶内仍残留一定量的SO2.围绕如何处理这些SO2的问题,同学们进行了相关探究.
[提出问题]SO2是形成酸雨的主要物质.由此想到,选用氢氧化钠等碱性溶液吸收SO2,效果会怎样?
[设计与实验]用两套完全相同的装置做对比实验(SO2不溶于植物油也不与其反应),如图所示:

(1)为确保实验的准确性,要先检查装置的
(2)实验开始叫,先用弹簧夹夹紧乳胶管,再将注射器内等体积的水和NaOH溶液分别注入充满SO2的集气瓶;
(3)充分吸收SO2后,打开弹簧夹,观察实验后进入两个集气瓶内植物油的体积.
[结论与解释])①把一片蓝色石蕊试纸放入盛有二氧化硫气体的集气瓶中,石蕊试纸没有变化②用胶头滴管吸取蒸馏水,滴在蓝色石蕊试纸上,试纸没有变化③把湿润的蓝色石蕊试纸放入盛有二氧化硫气体的集气瓶中,试纸变为红色
(1)甲实验中,SO2溶于水且与水反应生成H2SO3,反应的化学方程式为
(2)乙实验中,SO2与NaoH发生反应最终生成NaHSO3;
(3)分析实验现象得知,用碱性溶液比用水吸收SO2的效果
[拓展与迁移]
(1)在必须用煤作燃料的情况下.要减少SO2的排放,请你提出一条合理化建议
查看习题详情和答案>>
[提出问题]SO2是形成酸雨的主要物质.由此想到,选用氢氧化钠等碱性溶液吸收SO2,效果会怎样?
[设计与实验]用两套完全相同的装置做对比实验(SO2不溶于植物油也不与其反应),如图所示:

(1)为确保实验的准确性,要先检查装置的
气密性
;(2)实验开始叫,先用弹簧夹夹紧乳胶管,再将注射器内等体积的水和NaOH溶液分别注入充满SO2的集气瓶;
(3)充分吸收SO2后,打开弹簧夹,观察实验后进入两个集气瓶内植物油的体积.
[结论与解释])①把一片蓝色石蕊试纸放入盛有二氧化硫气体的集气瓶中,石蕊试纸没有变化②用胶头滴管吸取蒸馏水,滴在蓝色石蕊试纸上,试纸没有变化③把湿润的蓝色石蕊试纸放入盛有二氧化硫气体的集气瓶中,试纸变为红色
(1)甲实验中,SO2溶于水且与水反应生成H2SO3,反应的化学方程式为
SO2+H2O=H2SO3
;(2)乙实验中,SO2与NaoH发生反应最终生成NaHSO3;
(3)分析实验现象得知,用碱性溶液比用水吸收SO2的效果
好一些
.[拓展与迁移]
(1)在必须用煤作燃料的情况下.要减少SO2的排放,请你提出一条合理化建议
使用优质煤(或使用脱硫煤)
.