摘要:11.已知CO燃烧生成CO2.今有CO与H2的混合气体.其分子总数为N.则它们完全燃烧时.需要的氧气的分子数是
网址:http://m.1010jiajiao.com/timu_id_906223[举报]
 化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.
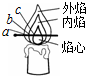
化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.(1)芳芳点燃蜡烛,观察到火焰分为外焰、内焰、焰心三层.把一根火柴梗放在火焰中(如图)约1s后取出可以看到火柴梗的
a
a
(填“a”、“b”或“c”)处最先碳化.结论:蜡烛火焰的外焰
外焰
温度最高;(2)三位同学在探究的过程中,将短玻璃导管插入焰心,发现另一端也可以点燃.导管里一定有可燃性气体,气体成分可能会是什么呢?
贝贝认为:可能是蜡烛不完全燃烧时产生的CO;
芳芳认为:可能是蜡烛受热后产生的石蜡蒸气;
婷婷认为:可能以上两种情况都有(注:CO可以燃烧生成CO2)
换一根较长的导管,并用冷的湿毛巾包住导管,然后在导管另一端做点火实验.
如果观察到
导管口能点燃,去掉毛巾,导管内壁看不到冷凝的固体
导管口能点燃,去掉毛巾,导管内壁看不到冷凝的固体
现象,则贝贝的猜想正确;如果观察到
导管口不能点燃,去掉毛巾,导管内壁可看到有冷凝的固体
导管口不能点燃,去掉毛巾,导管内壁可看到有冷凝的固体
现象,则芳芳的猜想正确;如果观察到
导管口能点燃,但火焰较小,去掉毛巾,导管内壁可看到有冷凝的固体
导管口能点燃,但火焰较小,去掉毛巾,导管内壁可看到有冷凝的固体
现象,则婷婷的猜想正确.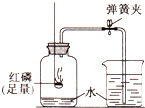 某同学用如图所示的装置测定空气中氧气的体积分数.
某同学用如图所示的装置测定空气中氧气的体积分数.(1)红磷燃烧时的现象为
发出黄光,放出热量,生成大量白烟
发出黄光,放出热量,生成大量白烟
,这一反应的文字表达式为磷+氧气
五氧化二磷
| 点燃 |
磷+氧气
五氧化二磷
.| 点燃 |
(2)当红磷熄灭并冷却到室温后,打开弹簧夹,观察到的现象是
烧杯中的水进入集气瓶,约占集气瓶剩余容积的
| 1 |
| 5 |
烧杯中的水进入集气瓶,约占集气瓶剩余容积的
,由此得出的结论是| 1 |
| 5 |
空气中的氧气约占空气气体的
| 1 |
| 5 |
空气中的氧气约占空气气体的
.| 1 |
| 5 |
(3)如果红磷熄灭后没有完全冷却到室温就打开弹簧夹,实验结果会偏低,其原因是
与室温相比,剩余气体温度较高,压强偏大,因此进入集气瓶中的水偏少
与室温相比,剩余气体温度较高,压强偏大,因此进入集气瓶中的水偏少
.(4)有人说:燃烧匙中红磷越多,进入集气瓶中的水就越多,你认为是否正确?
不正确,
不正确,
,其原因是空气中氧气的含量是一定的
空气中氧气的含量是一定的
.(5)通过本实验说明氮气的两点性质是
难溶于水
难溶于水
、不燃烧、不支持燃烧
不燃烧、不支持燃烧
.(6)已知木炭燃烧生成二氧化碳,有同学提出可以用木炭代替红磷测定空气中氧气的含量,你认为是否可以?
不可以
不可以
,理由是木炭燃烧生成的产物是二氧化碳气体,瓶内压强变化不大,不能测出空气中氧气的含量
木炭燃烧生成的产物是二氧化碳气体,瓶内压强变化不大,不能测出空气中氧气的含量
.几位同学发现村中池塘里不断地冒一些气泡,听人说这种气体可能是沼气,他们就上网搜索了相关资料:

①沼气是一种混合气体,可以燃烧.沼气是有机物经微生物厌氧消化而产生的可燃性气体;
②沼气是多种气体的混合物,一般含甲烷50%~70%,还含有CO2、N2和CO等.其特性与天然气相似;
③甲烷化学式为CH4,完全燃烧生成CO2和H2O.
为了检验气体的组成,他们设计了如图甲所示的取气方法:将空的雪碧汽水塑料瓶装满水,倒放在池塘水中,瓶口对准水底冒出的气泡进行收集.
(1)这种集气方法叫
(2)如图乙所示,若用水将瓶中的气体排出,水龙头应接导管
(3)他们将收集到的未知气体通过澄清石灰水,石灰水变浑浊,剩余气体通过浓硫酸(以上两步,能被吸收的气体均被完全吸收),再通入纯氧气中点燃,将燃烧后生成的气体依次通过无水硫酸铜、澄清石灰水,观察到无水硫酸铜变蓝,石灰水变浑浊.仅由以上实验现象分析此未知气体的组成,一定有的是(填化学式)
(4)①甲烷完全燃烧的化学方程式为
查看习题详情和答案>>

①沼气是一种混合气体,可以燃烧.沼气是有机物经微生物厌氧消化而产生的可燃性气体;
②沼气是多种气体的混合物,一般含甲烷50%~70%,还含有CO2、N2和CO等.其特性与天然气相似;
③甲烷化学式为CH4,完全燃烧生成CO2和H2O.
为了检验气体的组成,他们设计了如图甲所示的取气方法:将空的雪碧汽水塑料瓶装满水,倒放在池塘水中,瓶口对准水底冒出的气泡进行收集.
(1)这种集气方法叫
排水集气法
排水集气法
.针对瓶口太小不便收集的缺点,在不换瓶的情况下,你的改进方法是在瓶口加一漏斗
在瓶口加一漏斗
.(2)如图乙所示,若用水将瓶中的气体排出,水龙头应接导管
A
A
(填A或B).(3)他们将收集到的未知气体通过澄清石灰水,石灰水变浑浊,剩余气体通过浓硫酸(以上两步,能被吸收的气体均被完全吸收),再通入纯氧气中点燃,将燃烧后生成的气体依次通过无水硫酸铜、澄清石灰水,观察到无水硫酸铜变蓝,石灰水变浑浊.仅由以上实验现象分析此未知气体的组成,一定有的是(填化学式)
CO2、CH4
CO2、CH4
,不能确定其有无的是N2和CO
N2和CO
(填化学式).(4)①甲烷完全燃烧的化学方程式为
CH4+2O2
CO2+2H2O
| ||
CH4+2O2
CO2+2H2O
,②燃烧后的气体产物通入澄清石灰水变浑浊,涉及的化学反应方程式为
| ||
CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
.化学兴趣小组做蜡烛及其燃烧的探究实验.
(1)已知蜡烛燃烧生成水和二氧化碳,设计实验验证蜡烛燃烧的产物.
(2)蜡烛刚熄灭时会产生一股白烟,产生的白烟是什么呢?小明同学提出了如下假设:
A.白烟是蜡烛燃烧时生成的二氧化碳;
B.白烟是蜡烛燃烧时生成的水蒸气;
C.白烟是石蜡蒸气凝成的石蜡固体.
实验:①吹灭蜡烛,立即用一个沾有石灰水的烧杯罩住白烟,其目的是为了验证假设
②吹灭蜡烛,立即用一块干而冷的玻璃片放在白烟上,玻璃片上没有出现水雾,说明白烟不是
③吹灭蜡烛,立即用燃着的木条去点白烟(注意不要接触烛芯),发现蜡烛重新被点燃,说明白烟具有可燃性,这为假设
(3)事实证明,白烟是石蜡蒸气凝成的石蜡固体,可是为什么实验①中看到石灰水变浑浊了呢?
查看习题详情和答案>>
(1)已知蜡烛燃烧生成水和二氧化碳,设计实验验证蜡烛燃烧的产物.
| 实验目的 | 实验步骤 | 实验现象 |
| 证明有水生成 | ||
| 证明有二氧化碳生成 |
A.白烟是蜡烛燃烧时生成的二氧化碳;
B.白烟是蜡烛燃烧时生成的水蒸气;
C.白烟是石蜡蒸气凝成的石蜡固体.
实验:①吹灭蜡烛,立即用一个沾有石灰水的烧杯罩住白烟,其目的是为了验证假设
A
A
(填序号)②吹灭蜡烛,立即用一块干而冷的玻璃片放在白烟上,玻璃片上没有出现水雾,说明白烟不是
水蒸气
水蒸气
.③吹灭蜡烛,立即用燃着的木条去点白烟(注意不要接触烛芯),发现蜡烛重新被点燃,说明白烟具有可燃性,这为假设
C
C
(填序号)提供了证明,同时排除假设AB
AB
(填序号),因为二氧化碳和水蒸气不具有可燃性
二氧化碳和水蒸气不具有可燃性
.(3)事实证明,白烟是石蜡蒸气凝成的石蜡固体,可是为什么实验①中看到石灰水变浑浊了呢?