网址:http://m.1010jiajiao.com/timu_id_905236[举报]
 某安全火柴梗头及火柴盒侧面的物质如右图所示,当两者摩擦时,产生热量点燃红磷而使火柴梗着火.
某安全火柴梗头及火柴盒侧面的物质如右图所示,当两者摩擦时,产生热量点燃红磷而使火柴梗着火.请按要求填空:
(1)氯酸钾摩擦受热分解的化学方程式为
| ||
| △ |
| ||
| △ |
其中的二氧化锰的作用是
(2)红磷燃烧反应的化学方程式为
| ||
| ||

(1)由食用方法、贮藏指南中,可以推测到碘酸钾具有的化学性质之一是
(2)用单质碘(I2)与氯酸钾(KClO3)在一定条件下发生置换反应,可以制得碘酸钾(KIO3),该反应的化学方程式为
(3)国家质量检测部门在集贸市场某商店抽样检测该品牌500g袋装加碘食盐,经化验其中含碘酸钾30 mg,即含碘17.8 mg,则质量检测结论是
用下图回答
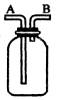
(1)①洗气:除去CO2中的水蒸气,装置内应盛的物质是 气体应从 端通入。
②检验:证明CO中含有CO2,装置里应感 ,要除去CO2,最好盛 。
③贮气:排空气法收集H2时,气体从 端通入,若要用水将装置中的O2排出进行实验,水应以 端通入
(2)某化学兴趣小组知道实验室也可用氯酸钾受热分解制取氧气,常使用MnO2作催化剂,该反应的化学方程式为:2KClO3 ![]() KCl+3O2↑。
KCl+3O2↑。
很想探究其他一些物质(如Fe2O3)是否也可以做KClO3分解的催化剂。请参与他们的探究过程,并填空。
①[提出问题]Fe2O3能不能做KClO3分解的催化剂?
②[猜想]Fe2O3能做KClO3分解的催化剂
③[实验验证]
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 取少量KClO3固体于试管中加热至溶化后,用带火星的木条伸入管口 | 加热KClO3需要很高的温度才能缓慢分解,产生O2 | |
| 实验二 | 取少量Fe2O3粉末于试管 中,加热较长时间后,用带 火星的木条伸入管口 | 木条不复燃 | |
| 实验三 | ①取少量KClO3固体于试管中,稍稍加热片刻,用带火星的木条伸入管口 | 木条不复燃 | |
| 把试管移开火焰,迅速撒入Fe2O3粉末,并用带火星的木条伸入管口 | 木条复燃 |
④[讨论与思考]经过讨论,有的同学认为只有上述几个实验证据还不能证明Fe2O3是KClO3分解的催化剂,需要补充一个探究实验,即将探究Fe2O3 。
(实验步骤)a.准确称量Fe2O3的质量。b.完成实验三。c.等试管冷却后,应进行的操作有 、 、洗涤、 、称量。d.对比反应前后Fe2O3的质量。
(讨论)多数同学认为,通过实验证明Fe2O3可以做KClO3分解的催化剂。但个别同学认为:要证明猜想,上述实验还不够,还需要增加一个探究实验,即探究Fe2O3的
.
查看习题详情和答案>>(1)写出助燃剂受热发生分解反应的化学方程式:
| ||
| △ |
| ||
| △ |
(2)气体甲的化学式:
(3)滤液加入硝酸银溶液发生反应的化学方程式:
| 配料 | 氯化钠、碘酸钾 |
| 含碘量 | (40~50mg)/kg |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避热、避光、密封、防潮 |
(2)由食用方法、贮藏指南中,可以推测到碘酸钾具有的化学性质之一是
(3)用单质碘(I2)与氯酸钾在一定条件下发生反应,可制得碘酸钾(KIO3),同时生成氯单质(Cl2).该反应的化学方程式为
(4)国家质量检测部门在集贸市场某商店抽样检测该品牌500g袋装加碘食盐,经化验其中含碘酸钾40mg,则含碘