网址:http://m.1010jiajiao.com/timu_id_904650[举报]
如图,A、B、C、D、E各代表铁、水、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质。常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D。请填空:
(1)写出下列物质的化学式:A ,B ,D 。
(2)相连环物质间发生的反应,没有涉及的基本反应类型是______________________。
54.(2008年镇江市)两种溶液混合,生成了一种沉淀。用酸碱盐的知识回答下列问题。
(1)若两种溶液均为无色,生成的白色沉淀不溶于稀硝酸,则两种溶液中的溶质可能是
和 ;
(2)若两种溶液均为无色,生成的白色沉淀溶于稀硝酸且有气体产生,则两种溶液中的溶质可能是 和 ;
(3)若一种溶液有色,另一种无色,生成的沉淀溶于稀盐酸且无气体产生,沉淀可能是_______
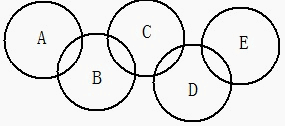
查看习题详情和答案>>(2008年自贡市)如图,A、B、C、D、E各代表铁、水、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质。常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D。请填空:
(1)写出下列物质的化学式:A ,B ,D 。
(2)相连环物质间发生的反应,没有涉及的基本反应类型是______________________。
54.(2008年镇江市)两种溶液混合,生成了一种沉淀。用酸碱盐的知识回答下列问题。
(1)若两种溶液均为无色,生成的白色沉淀不溶于稀硝酸,则两种溶液中的溶质可能是
和 ;
(2)若两种溶液均为无色,生成的白色沉淀溶于稀硝酸且有气体产生,则两种溶液中的溶质可能是 和 ;
(3)若一种溶液有色,另一种无色,生成的沉淀溶于稀盐酸且无气体产生,沉淀可能是_______
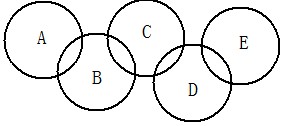
(2008年自贡市)如图,A、B、C、D、E各代表铁、水、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质。常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D。请填空:
(1)写出下列物质的化学式:A ,B ,D 。
(2)相连环物质间发生的反应,没有涉及的基本反应类型是______________________。
54.(2008年镇江市)两种溶液混合,生成了一种沉淀。用酸碱盐的知识回答下列问题。
(1)若两种溶液均为无色,生成的白色沉淀不溶于稀硝酸,则两种溶液中的溶质可能是
和 ;
(2)若两种溶液均为无色,生成的白色沉淀溶于稀硝酸且有气体产生,则两种溶液中的溶质可能是 和 ;
(3)若一种溶液有色,另一种无色,生成的沉淀溶于稀盐酸且无气体产生,沉淀可能是_______
材料:2013年12月2日,“嫦娥三号”探测器由长征三号运载火箭发射,首次实现月球软着陆和月面巡视勘察。12月15日晚,“嫦娥三号”着陆器和巡视器(玉兔月球车)成功分离,顺利互拍,任务取得圆满成功。长征三号运载火箭主要用于发射地球同步轨道有效载荷,它的一子级和二子级使用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作推进剂,三子级则使用效能更高的液氢(H2)和液氧(O2)。
(1)“长征三号”三子级火箭用液氢做燃料,其反应的化学方程式为 ,使用液氢做燃料的优点有: (填一条)。
(2)下列有关偏二甲肼(C2H8N2)的叙述正确的是
| A.由2个碳原子,4个氢原子,一个氮分子组成 |
| B.由碳、氢、氮三种元素组成 |
| C.由2个碳原子,8个氢原子,2个氮原子构成 |
| D.偏二甲肼中碳、氢、氮的原子个数比为1:4:1 |

(4)看见玉兔车金灿灿的车身后,小聪想到家里新换的水龙头。从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,请你一同参加。
【知识回放】
金属活动性顺序:K Ca Na Al Zn Fe Sn Pb(H)Cu Ag Pt Au。请你在横线上填写对应金属的元素符号。
【作出猜想】
猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu >Cr; 猜想3.你的猜想是 。
【查阅资料】
①铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 | 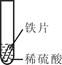 | 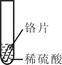 | 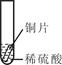 |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | |
【结论与解释】
①小聪得到的结论是猜想 正确。
②实验前用砂纸打磨金属片的目的是 。
【知识运用】
将铬片投入FeSO4溶液中,反应 (填“能”或“不能”)进行。若能进行,请你写出反应的化学方程式 。 查看习题详情和答案>>
【实验探究一】同学们发现鸡蛋放置时间太久会变质并会产生一股臭味,这是什么原因呢?
查阅资料:
①鸡蛋久置后会变质产生硫化氢(H2S)气体;硫化氢气体有剧毒,密度比空气大,能溶于水,溶于水后呈酸性.
②实验室可用硫化亚铁(化学式为FeS)固体和稀硫酸在常温下反应来制取硫化氢气体,同时生成硫酸亚铁;
同学们在实验室制取并收集了一瓶硫化氢气体,回答下列问题:
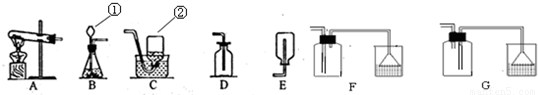
(1)写出有标号的仪器的名称
① ②
(2)H2S气体中的硫元素的化合价为 ,写出实验室制取硫化氢气体的化学方程式 ,该反应属于 反应(填基本反应类型),制取该气体应选用的发生装置为 (填字母),收集硫化氢气体最好选用的装置为 (填字母),多余的气体可用 溶液来吸收.
【实验探究二】鸡蛋壳的成分
(注意:以下实验均假设鸡蛋壳中除碳酸钙以外的其他成分不能与酸反应,也不溶于水)
(3)小李同学查知鸡蛋壳的主要成份是碳酸钙,他用镊子取少许鸡蛋壳样品在酒精灯上灼烧,一开始闻到一股烧焦羽毛气味,说明内膜有 ,继续灼烧后,看到蛋壳边变白,产生该白色物质的化学反应方程式为 ,将充分灼烧后的蛋壳投入蒸馏水中,滴入无色酚酞试液,试液变为 色,发生反应的化学方程式为 .
(4)为了进一步测定蛋壳中碳酸钙的质量分数,小刚同学进行了如下实验.
称量G装置质量为50.00g,按下图组装后,将10.00g蛋壳样品(已洗净、干燥并捣碎)放入锥形瓶中,加入足量稀盐酸,待锥形瓶中不再产生气泡时,打开弹簧夹C,从导管A处缓缓鼓入空气,一段时间后称量装置G质量为52.64g(不考虑原装置内空气对实验的影响).
回答下列问题:
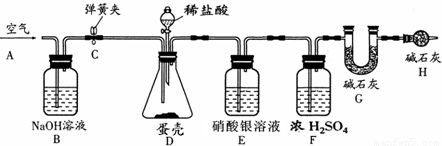
加入样品前还应 ,装置D中反应的化学方程式为 ,装置E的作用是 ,反应结束后打开弹簧夹C,缓缓鼓入空气的目的是 ,装置B的作用是 ,若缺少H装置,则测得的碳酸钙的质量分数将偏 .小刚的实验测得蛋壳中碳酸钙的质量分数为 .
(5)小勇同学重新设计了一种方案,将10.00g蛋壳样品(已洗净、干燥并捣碎)放在烧杯里,然后往烧杯中加入足量稀盐酸,蛋壳部分溶解,并产生大量气泡,实验过程和测定的相关实验数据如下所示:

小勇的实验测得蛋壳中碳酸钙的质量分数为 ,小刚认为小勇的实验过程有一个明显的缺陷会导致测得的碳酸钙的含量偏低,这个缺陷是 . 查看习题详情和答案>>