摘要:水溶液中的溶质在水中的存在形式是A.人的肉眼看不见的细小颗粒 B.分子C.离子 D.分子或离子
网址:http://m.1010jiajiao.com/timu_id_903695[举报]
已知海水中镁元素主要以氯化镁的形式存在,其质量分数仅次于氯元素和钠元素,氯化镁能和常见的碱发生复分解反应.目前世界上的大部分镁来自于海水.甲、乙、丙三位同学欲测定海水中氯化镁的含量,分别进行了如下实验,数据如表,已知其中只有一位同学用的海水样品与所加入的氢氧化钠溶液恰好完全反应.
则:(1)两溶液恰好完全反应的实验是(填“甲”或“乙”或“丙”) 实验
(2)计算海水样品中MgCl2的质量分数.(保留三位小数) 查看习题详情和答案>>
| 甲 | 乙 | 丙 | |
| 所取海水样品的质量(g) | 200 | 200 | 300 |
| 加入NaOH溶液的质量(g) | 40 | 20 | 20 |
| 反应后所得沉淀物的质量(g) | 0.58 | 0.58 | 0.58 |
(2)计算海水样品中MgCl2的质量分数.(保留三位小数) 查看习题详情和答案>>
139、碱溶液具有许多共同性质的原因是,碱在水溶液中都能电离出
①能与酸碱指示剂作用:能使紫色石蕊试液变
注意:对于难溶的弱碱如:Cu(OH)2、Fe(OH)3、Al(OH)3、Mg(OH)2,由于在溶液中难电离,不能形成溶液,所以不能与酸碱指示剂作用.
②(p190)能与某些非金属氧化物反应生成
分别写出CO2与NaOH、Ca(OH)2反应的化学方程式:CO2+2NaOH=Na2CO3+H2O,CO2+Ca(OH)2=CaCO3↓+H2O
固体NaOH必须密封保存的原因是
③能与某些盐反应生成
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,CuSO4+Ca(OH)2=Cu(OH)2↓+CaSO4
其中,CuSO4与Ca(OH)2的反应是农业上配制
写出Na2CO3与Ca(OH)2反应的化学方程式
④碱能与酸发生中和反应
查看习题详情和答案>>
OH-
,碱的化学性质如下:①能与酸碱指示剂作用:能使紫色石蕊试液变
蓝
,无色的酚酞试液变红
.注意:对于难溶的弱碱如:Cu(OH)2、Fe(OH)3、Al(OH)3、Mg(OH)2,由于在溶液中难电离,不能形成溶液,所以不能与酸碱指示剂作用.
②(p190)能与某些非金属氧化物反应生成
盐
和水
.分别写出CO2与NaOH、Ca(OH)2反应的化学方程式:CO2+2NaOH=Na2CO3+H2O,CO2+Ca(OH)2=CaCO3↓+H2O
固体NaOH必须密封保存的原因是
能够吸收空气中的水分
,能和二氧化碳反应
.③能与某些盐反应生成
碱
和盐
.分别写出CuSO4溶液与NaOH溶液、Ca(OH)2溶液反应的化学方程式:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,CuSO4+Ca(OH)2=Cu(OH)2↓+CaSO4
其中,CuSO4与Ca(OH)2的反应是农业上配制
波尔多液
的主要反应.写出Na2CO3与Ca(OH)2反应的化学方程式
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
.④碱能与酸发生中和反应
CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.小平和小明同学用这种大理石和稀盐酸反应,分别开展以下探究,请你参与探究并回答相关问题.
[查阅资料]资料一:在常温下,测得浓度均为a%的下列六种溶液的pH大小情况:
| 溶质 | H2SO4 | HCl | H2S | H2CO3 | HClO |
| pH | 小→大 | ||||
A.H2SO4+2NaHCO3=2NaCl+2H2O+2CO2↑ B.2HCl+CaS=CaC2l+H2S↑
C.CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D.H2S+CuSO4=H2SO4+CuS↓
资料二:CuS是黑褐色无定形粉末或粒状物,不溶于浓盐酸,不溶于水和硫化钠溶液.
[实验探究]小平同学为了得到纯净的二氧化碳,设计了如下装置,请你分析:
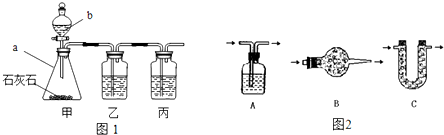
[制取CO2]利用图1、与图2干燥装置制得纯净干燥的CO2.
(1)仪器a的名称是________,仪器b的名称是________.装置甲中主要反应的化学方程式为________.
(2)装置丙盛有足量的饱和NaHCO3溶液,目的是除去________.装置丙中主要反应的化学方程式为________.装置乙中盛有的物质是________溶液.现象:________.
(3)利用图2干燥装置干燥气体,常见干燥剂有①浓硫酸②无水氯化钙③碱石灰④生石灰若选用A装置,则A装置中放入药品________(选择序号);若选用B装置,则B装置中放入药品________(选择序号).
(4)小明同学为了计算这种大理石中含碳酸钙质量分数,进行了如下定量实验:
| 实验步骤 | I将适量盐酸加入烧杯中并称量 | II称取少量大理石样品加入烧杯中,使之与过量稀盐酸反应 | III待反应完全后,称重 |
| 实验图示 |  | ||
| 实验数据 | 烧杯和盐酸的质量为100.0g | 大理石样的质量为12.0g | 烧杯和其中混合物的质量为107.6g |