网址:http://m.1010jiajiao.com/timu_id_898672[举报]
实验室常用过氧化氢溶液和用二氧化锰作催化剂制取氧气。
【提出问题】二氧化锰是催化剂,二氧化锰的用量对反应速率是否有影响?
【设计实验】(1)实验装置如图所示。

(2)实验记录:每次用30mL10%的过氧化氢溶液,采用不同量二氧化锰粉末做催化剂进行实验,测定相关数据记录于下表中:
|
序号 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
MnO2(g) |
0.1 |
0.2 |
0.3 |
0.4 |
0.5 |
0.6 |
0.7 |
0.8 |
0.9 |
1.0 |
|
待测数据 |
|
|
|
|
|
|
|
|
|
|
【分析】(1)写出该反应的符号表达式 。
(2)上述实验应该测定的“待测数据”可能是 。
(3)10次实验“每次用30 mL 10%的过氧化氢溶液”的目的是 。
(4)若第2次实验比第3次实验的“待测数据”更 (填"大"或"小"),说明催化剂的用量越多,反应越快。
【实验与结果】经多次实验证明,第1次实验至第7次实验中过氧化氢的分解速率依次加快,第7次实验至第10次实验所记录的“待测数据”无明显差异。
【结论】 。
【评价与反思】(答对本小题奖励4分,化学试卷总分不超过60分)
氧化铜是否也能用做过氧化氢溶液制取氧气的催化剂?请设计实验验证。
。
查看习题详情和答案>>
实验室常用过氧化氢溶液和用二氧化锰作催化剂制取氧气。
【提出问题】二氧化锰是催化剂,二氧化锰的用量对反应速率是否有影响?
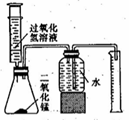
【设计实验】(1)实验装置如右图所示。
(2)实验记录:每次用30mL10%的过氧化氢溶液,采用不同量二氧化锰粉末做催化剂进行实验,测定相关数据记录于下表中:
| 序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 待测数据 |
【分析】(1)写出该反应的符号表达式 。
(2)上述实验应该测定的“待测数据”可能是 。
(3)10次实验“每次用30 mL 10%的过氧化氢溶液”的目的是 。
(4)若第2次实验比第3次实验的“待测数据”更 (填"大"或"小"),说明催化剂的用量越多,反应越快。
【实验与结果】经多次实验证明,第1次实验至第7次实验中过氧化氢的分解速率依次加快,第7次实验至第10次实验所记录的“待测数据”无明显差异。
【结论】 。
【评价与反思】(答对本小题奖励4分,化学试卷总分不超过60分)
氧化铜是否也能用做过氧化氢溶液制取氧气的催化剂?请设计实验验证。
。
查看习题详情和答案>>常用过氧化氢溶液和用二氧化锰作催化剂制取氧气。
【提出问题】二氧化锰是催化剂,二氧化锰的用量对反应速率是否有影响?
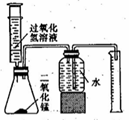
【设计实验】(1)实验装置如右图所示。
(2)实验记录:每次用30mL10%的过氧化氢溶液,采用不同量二氧化锰粉末做催化剂进行实验,测定相关数据记录于下表中:
| 序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 待测数据 |
【分析】(1)写出该反应的符号表达式 。
(2)上述实验应该测定的“待测数据”可能是 。
(3)10次实验“每次用30 mL 10%的过氧化氢溶液”的目的是 。
(4)若第2次实验比第3次实验的“待测数据”更 (填"大"或"小"),说明催化剂的用量越多,反应越快。
【实验与结果】经多次实验证明,第1次实验至第7次实验中过氧化氢的分解速率依次加快,第7次实验至第10次实验所记录的“待测数据”无明显差异。
【结论】 。
【评价与反思】(答对本小题奖励4分,化学试卷总分不超过60分)
氧化铜是否也能用做过氧化氢溶液制取氧气的催化剂?请设计实验验证。
。
(1)根据上面叙述,归纳写出碳酸氢铵的性质.
①
(2)草木灰含有碳酸钾(其水溶液能使无色酚酞试液变红色).从草木灰中提取碳酸钾的步骤为:
(3)某农民发现他种植的农作物植株矮小,叶片发黄,茎杆软弱,容易倒伏,叶片的边缘和尖端呈黄褐色并逐渐焦枯,于是他决定将碳酸氢铵与草木灰混合施用,以补充植物所缺乏的氮元素和钾元素.则该农民的判断是否准确?

(1)写出带标号仪器的名称:①
(2)用高锰酸钾制取O2时,其反应的表达式为:
| 加热 |
| 加热 |
①应采用
②可采用C装置收集O2,理由
③也可以采用
(3)过氧化氢俗称双氧水,是一种无色液体,在少量二氧化锰作为
该反应的表达式为:
| 二氧化锰 |
| 二氧化锰 |
(4)实验室常用大理石和稀盐酸制取CO2,选用
(5)实验室用块状固体硫化亚铁(FeS)与稀硫酸反应制取硫化氢(H2S)气体,硫化氢气体的密度比空气的密度大,能溶于水形成氢硫酸.根据以上知识推断:实验室制取硫化氢气体应选用的发生装置为