摘要:若将溶液降温到200℃时.可观察到的现象是 , .若要看到塑料板上浮.应采用的方法是 .
网址:http://m.1010jiajiao.com/timu_id_894531[举报]
图1是甲、乙两种物质的溶解度曲线,图2所示两个烧杯中各盛有20℃时上述两种物质的饱和溶液。请你通过分析,回答下列问题:
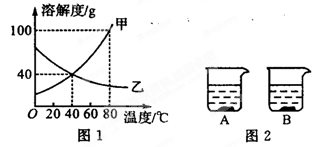
(1)溶解度随温度升高而增大的物质是 (填“甲”或“乙”);
(2)80℃时,100 g水中最多可溶解甲物质 g,该饱和溶液中溶质的质量分数为 。
(3)当温度由20℃升高至60℃时(不考虑水分蒸发),B烧杯中固体质量增加,则B烧杯溶液中的溶质是 (填“甲”或“乙”)。
(4)由图1分析,若分别将200 g甲、乙的饱和溶液从80℃降温到40℃,对所得溶液的叙述正确的是 (填序号)。
A.甲、乙都是饱和溶液 B.所含溶剂质量:甲<乙
C.溶液质量:甲>乙 D.溶质质量分数:甲>乙
(5)甲中混有少量乙,如果要提纯甲,分离的实验操作步骤主要有:①称量需提纯的固体混合物;②控制水量,配制成80℃左右的饱和溶液; ③降温至20℃后进行过滤,并用少量冷水洗涤过滤器中的固体2-3次;④取出固体,干燥、包装。
请回答:步骤③中,过滤后,需进行洗涤,目的是 。
不用热水而用冷水洗涤的原因是 。
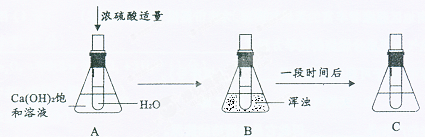
(6)有同学做了以下实验,请仔细观察下图中实验过程和溶液的变化并回答问题。
在A、B、C 中Ca(OH)2 溶液的溶质质量分数的大小关系是 。

(1)溶解度随温度升高而增大的物质是 (填“甲”或“乙”);
(2)80℃时,100 g水中最多可溶解甲物质 g,该饱和溶液中溶质的质量分数为 。
(3)当温度由20℃升高至60℃时(不考虑水分蒸发),B烧杯中固体质量增加,则B烧杯溶液中的溶质是 (填“甲”或“乙”)。
(4)由图1分析,若分别将200 g甲、乙的饱和溶液从80℃降温到40℃,对所得溶液的叙述正确的是 (填序号)。
A.甲、乙都是饱和溶液 B.所含溶剂质量:甲<乙
C.溶液质量:甲>乙 D.溶质质量分数:甲>乙
(5)甲中混有少量乙,如果要提纯甲,分离的实验操作步骤主要有:①称量需提纯的固体混合物;②控制水量,配制成80℃左右的饱和溶液; ③降温至20℃后进行过滤,并用少量冷水洗涤过滤器中的固体2-3次;④取出固体,干燥、包装。
请回答:步骤③中,过滤后,需进行洗涤,目的是 。
不用热水而用冷水洗涤的原因是 。
(6)有同学做了以下实验,请仔细观察下图中实验过程和溶液的变化并回答问题。
在A、B、C 中Ca(OH)2 溶液的溶质质量分数的大小关系是 。

 28、物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.
28、物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.【方案一】:先在NaOH稀溶液中滴加几滴酚酞试液,溶液显
红
色,然后再滴加盐酸,当观察到红色褪去
,证明NaOH溶液与稀盐酸发生了化学反应.当得到无色溶液时,小虎认为这时酸与碱恰好完全反应.小英却认为这时还应该存在的另一种情况是盐酸过量
.接着老师又提出问题:红色消失一定证明是酸与碱发生中和反应吗?他们经过讨论认为也可能是酚酞与酸反应而褪色.这时应在溶液中再滴加酚酞(或氢氧化钠溶液)
溶液,若有不变红(或变红)
现象,则证明不是酚酞与酸反应而褪色.【方案二】:用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明NaOH溶液与稀盐酸发生了化学反应.这时小虎又提出疑问:pH逐渐变小,可能是由于溶液稀释造成的,不能说明一定发生了反应.小全对小虎的疑问进行了反驳,他的理由是:
碱溶液无论如何稀释,其pH值都不可能小于7
.测定溶液的pH时,需在白瓷板或玻璃片上放一小片pH试纸,用
滴管或玻璃棒
把待测液滴在pH试纸上,过一会儿,将试纸的颜色与标准比色卡
比较,从而得出溶液的pH.若对一未知溶液用湿润的pH试纸来测定溶液的pH,则测定的结果会D
.A.偏大,B.偏小,C.不变,D.以上三种可能都有
【方案三】:在试管中放入一粒NaOH固体,然后加入稀盐酸.
小华看到氢氧化钠固体消失了,认为发生了反应.而小全想了想之后却不同意小华的观点,小全的理由是:
可能是氢氧化钠溶于水
.小明用手摸了摸试管外壁,试管比较热,他认为不仅说明它们发生了反应,而且是放热反应.小全思考之后仍然不同意小明的观点,小全的理由是:氢氧化钠溶于水也放热
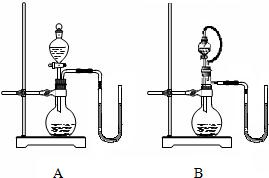
.乙同学和丙同学各设计了一个装置(见右图),都说在不使用温度计的情况下可以判断NaOH溶液与稀盐酸发生了中和反应.分析说明:
B
(填序号)装置更合理,理由是B装置能排除因液体的滴入而造成烧瓶内气体排出,引起玻璃管内液面发生变化
.若选用合理的装置进行实验,当出现玻璃管中左侧液面下降,右侧液面上升
现象时,可以说明NaOH溶液与稀盐酸发生了反应.【方案四】:可以通过测定反应前的物质不存在来判断反应的发生.将一定量的稀盐酸溶液平均分为两份,一份直接加入锌粒中,观察到的现象是
有气泡产生
;向另一份中先加入过量的NaOH溶液,再加入锌粒中,观察到无气泡产生
现象,说明NaOH溶液和HCl溶液发生了反应.锌粒与稀盐酸反应的化学方程式为Zn+2HCl═ZnCl2+H2↑
.【方案五】:定量研究是化学研究中的一种重要的方法.一同学将200 mL稀盐酸平均分成两份,其中一份直接加入到w g的CaCO3中,充分反应后收集到V1体积的CO2;向另一份中先滴加一定量的NaOH溶液,充分反应后,也加入到w g的CaCO3中,反应后收集到V2体积的CO2.如果V1
>
V2(填“>”或“<”或“=”)也能说明NaOH溶液和HCl溶液发生了反应.