网址:http://m.1010jiajiao.com/timu_id_891408[举报]
(1)选择药品.小明对三组药品进行了研究,实验记录如下:
| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
(2)选择装置.他认为能选择用过氧化氢制氧气的发生装置.你认为他选择气体发生装置的依据是
(3)制取气体.将药品装入所选装置制取气体,他认为只能用向上排空气法收集,是因为
(4)气体检验.将生成的气体通入石蕊中,石蕊变红.原因是(用反应的文字表达式表示)
(5)提供简易装置完成二氧化碳的制取、收集和验满.
如图是实验桌上摆放好的该实验所需用品,小明发现缺少一种实验仪器和一种药品,仪器名称
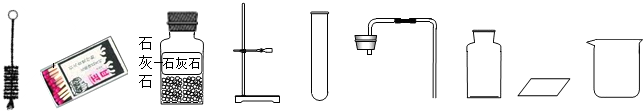
(6)如图(1)是小明实验的主要步骤,这些步骤的正确顺序是
(7)如果在实验过程中要向试管中添加酸溶液,要求不改变实验装置,可选用
(8)如果要用上述仪器完成用高锰酸钾制取氧气,还需增加的玻璃仪器是
| 加热 |
| 加热 |
(9)用如图(2)所示装置收集二氧化碳,则应该从
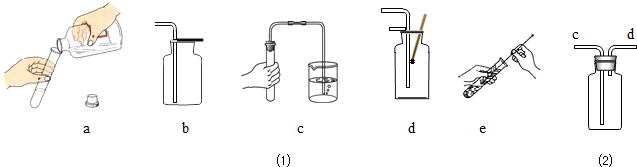
下图所示为实验室常用的实验装置:
 (1)写出下列仪器名称:a ;b 。
(1)写出下列仪器名称:a ;b 。
(2)实验室用高锰酸钾制取氧气时,应选择的发生装置和收集装置是 (填装置的字母代号),化学方程式 ,实验室制取二氧化碳的原料是 ,化学方程式 ,
用D装 置收集气体时集满的实验现象是 ,
置收集气体时集满的实验现象是 ,
(3)若用E装置收集氢气,则氢气应从 口通入(填c或d)。
(4)F装置可用来测量生成的CO2气体的体积,在水面上放一层植物油的目的是 。
(5)装置C相对于装置B在操作方面的优势为: 。
(6)某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止。为此该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳。
[实验一] 选择合适浓度的硫酸
操作:在28℃时,分别用装有5mL不同浓度硫酸溶液的注射器向盛有1g直径为2mm大理石细小颗粒的大试管中注入硫酸,记录15分钟内生成气体的体积,见下表:
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度 | 15% | 20% | 25% | 30% | 35% |
| 气体体积/mL | 35 | 47 | 55 | 51 | 42 |
[实验二] 选择合适的反应温度
操作:往盛有1g直径为2mm大理石细小颗粒的大试管中分别加入5mL相同合适浓度而不同温度的硫酸溶液,观察反应的情况,记录如下表:
| 试管编号 | A | B | C | D | E |
| 温度(℃) | 40 | 50 | 60 | 70 | 80 |
| 现象和 | 有少量气泡 | 气泡比A号试管多 | 气泡明显比B号试管多 | 大量气泡产生,与常温用盐酸反应相似 | 反应激烈,迅速产生大量气体 |
请根据本次活动的研究目的,分析处理以上两个表中数据,得出结论:
①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适为 ,因为浓度小于或大于此浓度对反应的影响是 。
② 在合适的硫酸浓度下,应选择最合适的反应温度为 ℃。
在合适的硫酸浓度下,应选择最合适的反应温度为 ℃。
③除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加 操作,更有利于气体的制备。
④该研究小组为了研究 对该反应速率的影响,在28℃进行了如下实验。
| 试管编号 | A | B |
| 试管内药品 | 1g块状大理石与5mL25%稀硫酸 | 1g细小颗粒大理石与5mL25%稀硫酸 |
| 现象和比较 | 有少量气泡 | 迅速产生较多气泡 |
根据上述实验研究,你觉得在以下硫酸和大理石反应的装置中,最佳选用 (填
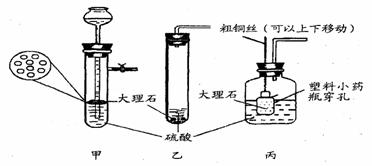 编号) .
编号) .
下图所示为实验室常用的实验装置:
(1)写出下列仪器名称:a ;b 。
(2)实验室用高锰酸钾制取氧气时,应选择的发生装置和收集装置是 (填装置的字母代号),化学方程式 ,实验室制取二氧化碳的原料是 ,化学方程式 ,用D装置收集气体时集满的实验现象是 ,
(3)若用E装置收集氢气,则氢气应从 口通入(填c或d)。
(4)F装置可用来测量生成的CO2气体的体积,在水面上放一层植物油的目的是 。
(5)装置C相对于装置B在操作方面的优势为: 。
(6)某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止。为此该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳。
[实验一] 选择合适浓度的硫酸
操作:在28℃时,分别用装有5mL不同浓度硫酸溶液的注射器向盛有1g直径为2mm大理石细小颗粒的大试管中注入硫酸,记录15分钟内生成气体的体积,见下表:
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度 | 15% | 20% | 25% | 30% | 35% |
| 气体体积/mL | 35 | 47 | 55 | 51 | 42 |
操作:往盛有1g直径为2mm大理石细小颗粒的大试管中分别加入5mL相同合适浓度而不同温度的硫酸溶液,观察反应的情况,记录如下表:
| 试管编号 | A | B | C | D | E |
| 温度(℃) | 40 | 50 | 60 | 70 | 80 |
| 现象和 比较 | 有少量气泡 | 气泡比A号试管多 | 气泡明显比B号试管多 | 大量气泡产生,与常温用盐酸反应相似 | 反应激烈,迅速产生大量气体 |
①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适为 ,因为浓度小于或大于此浓度对反应的影响是 。
②在合适的硫酸浓度下,应选择最合适的反应温度为 ℃。
③除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加 操作,更有利于气体的制备。
④该研究小组为了研究 对该反应速率的影响,在28℃进行了如下实验。
| 试管编号 | A | B |
| 试管内药品 | 1g块状大理石与5mL25%稀硫酸 | 1g细小颗粒大理石与5mL25%稀硫酸 |
| 现象和比较 | 有少量气泡 | 迅速产生较多气泡 |
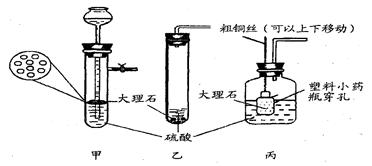 查看习题详情和答案>>
查看习题详情和答案>>
(1)选择药品.小明对三组药品进行了研究,实验记录如下:
| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
(2)选择装置.他认为能选择用过氧化氢制氧气的发生装置.你认为他选择气体发生装置的依据是______
(3)制取气体.将药品装入所选装置制取气体,他认为只能用向上排空气法收集,是因为______
(4)气体检验.将生成的气体通入石蕊中,石蕊变红.原因是(用反应的文字表达式表示)______.由此实验他确定该气体一定是二氧化碳.他的检验方法是否正确?请说明理由______
(5)提供简易装置完成二氧化碳的制取、收集和验满.
如图是实验桌上摆放好的该实验所需用品,小明发现缺少一种实验仪器和一种药品,仪器名称______;药品名称______
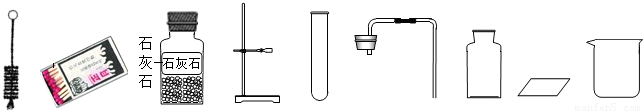
(6)如图(1)是小明实验的主要步骤,这些步骤的正确顺序是______(填字母序号),其中操作有误的是______
(7)如果在实验过程中要向试管中添加酸溶液,要求不改变实验装置,可选用______来完成.
(8)如果要用上述仪器完成用高锰酸钾制取氧气,还需增加的玻璃仪器是______文字表达式______ 查看习题详情和答案>>
下图所示为实验室常用的实验装置:

(1)写出下列仪器名称:a ;b 。
(2)实验室用高锰酸钾制取氧气时,应选择的发生装置和收集装置是 (填装置的字母代号),化学方程式 ,实验室制取二氧化碳的原料是 ,化学方程式 ,用D装置收集气体时集满的实验现象是 ,
(3)若用E装置收集氢气,则氢气应从 口通入(填c或d)。
(4)F装置可用来测量生成的CO2气体的体积,在水面上放一层植物油的目的是 。
(5)装置C相对于装置B在操作方面的优势为: 。
(6)某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止。为此该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳。
[实验一] 选择合适浓度的硫酸
操作:在28℃时,分别用装有5mL不同浓度硫酸溶液的注射器向盛有1g直径为2mm大理石细小颗粒的大试管中注入硫酸,记录15分钟内生成气体的体积,见下表:
|
试管编号 |
1 |
2 |
3 |
4 |
5 |
|
硫酸浓度 |
15% |
20% |
25% |
30% |
35% |
|
气体体积/mL |
35 |
47 |
55 |
51 |
42 |
[实验二] 选择合适的反应温度
操作:往盛有1g直径为2mm大理石细小颗粒的大试管中分别加入5mL相同合适浓度而不同温度的硫酸溶液,观察反应的情况,记录如下表:
|
试管编号 |
A |
B |
C |
D |
E |
|
温度(℃) |
40 |
50 |
60 |
70 |
80 |
|
现象和 比较 |
有少量气泡 |
气泡比A号试管多 |
气泡明显比B号试管多 |
大量气泡产生,与常温用盐酸反应相似 |
反应激烈,迅速产生大量气体 |
请根据本次活动的研究目的,分析处理以上两个表中数据,得出结论:
①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适为 ,因为浓度小于或大于此浓度对反应的影响是 。
②在合适的硫酸浓度下,应选择最合适的反应温度为 ℃。
③除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加 操作,更有利于气体的制备。
④该研究小组为了研究 对该反应速率的影响,在28℃进行了如下实验。
|
试管编号 |
A |
B |
|
试管内药品 |
1g块状大理石与5mL25%稀硫酸 |
1g细小颗粒大理石与5mL25%稀硫酸 |
|
现象和比较 |
有少量气泡 |
迅速产生较多气泡 |
根据上述实验研究,你觉得在以下硫酸和大理石反应的装置中,最佳选用 (填编号) .

查看习题详情和答案>>