摘要:8.同学们相信你们有下面的生物知识吧: 叶绿体 酶
网址:http://m.1010jiajiao.com/timu_id_885215[举报]
同学们相信你们有下面的生物知识吧:则两个变化中有机物的化学式为( )
①绿色植物在光照时主要进行光合作用,其过程为:6CO2+6H2O
有机物+6O2
②绿色植物在避光时主要进行呼吸作用,其过程为:有机物+6O2
6CO2+6H2O.
①绿色植物在光照时主要进行光合作用,其过程为:6CO2+6H2O
| ||
| 叶绿体 |
②绿色植物在避光时主要进行呼吸作用,其过程为:有机物+6O2
| 酶 |
| A、C2H5OH |
| B、CH4 |
| C、C6H12O6 |
| D、CH3COOH |
同学们相信你们有下面的生物知识吧:则两个变化中有机物的化学式为( )
①绿色植物在光照时主要进行光合作用,其过程为:6CO2+6H2O 有机物+6O2
有机物+6O2
②绿色植物在避光时主要进行呼吸作用,其过程为:有机物+6O2 6CO2+6H2O.
6CO2+6H2O.
A.C2H5OH
B.CH4
C.C6H12O6
D.CH3COOH
查看习题详情和答案>>
①绿色植物在光照时主要进行光合作用,其过程为:6CO2+6H2O
 有机物+6O2
有机物+6O2②绿色植物在避光时主要进行呼吸作用,其过程为:有机物+6O2
 6CO2+6H2O.
6CO2+6H2O.A.C2H5OH
B.CH4
C.C6H12O6
D.CH3COOH
查看习题详情和答案>>
同学们相信你们有下面的生物知识吧:则两个变化中有机物的化学式为
①绿色植物在光照时主要进行光合作用,其过程为:6CO2+6H2O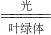 有机物+6O2
有机物+6O2
②绿色植物在避光时主要进行呼吸作用,其过程为:有机物+6O2 6CO2+6H2O.
6CO2+6H2O.
- A.C2H5OH
- B.CH4
- C.C6H12O6
- D.CH3COOH
同学们在化学实验室发现,盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末.
[提出问题]盛放NaOH溶液的试剂瓶瓶口的白色粉末究竟是什么物质?
[查阅资料](1)已知玻璃的主要成分是二氧化硅(Si02),它具能与CO2、SO2相似的化学性质,与氢氧化钠反应产生的硅酸钠(Na2SiO3)和水,硅酸钠也是一种白色固体,俗称“水玻璃”,它是一种凝胶,能将玻璃粘结在一起;
(2)硅酸钠和盐酸或硫酸能发生复分解反应,产生的硅酸(H2SiO3)是一种白色难溶解于水的固体.
[成分分析]同学们依据所学的化学知识结合从资料中获取的信息,对这种白色粉末的成分作了如下猜想:
①小军可能是Na2CO3和Na2SiO3的混合物;
②小红可能是NaOH、Na2CO3和Na2SiO3的混合物.
[实验验证]为了验证猜想,小红同学取少量上述白色粉末并完全溶于水,用pH试纸测得溶液的pH大于7,继续向溶液中滴加稀盐酸至过量,发现有气体生成,同时还有白色沉淀出现.由此小红认为自己的猜想成立.
(1)写出下列有关化学反应的化学方程式:
①二氧化硅(Si02)和氢氧化钠溶液的反应 ;
②小红的实验中,白色沉淀形成的化学反应 .
[问题解答]
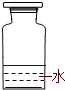
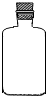
(2)实验室里不同化学试剂的保存方法不尽相同.现有①NaOH溶液、②硝酸银溶液、③大理石、④白磷、⑤稀硫酸等5种药品可分别保存在下列各试剂瓶中,请把NaOH溶液和硝酸银溶液的序号填写在各试剂瓶下面的括号内:
(3)老师和同学们都认为小红所得结论不正确,为什么? .
[含量测定]在老师的指导下,同学们设计了实验并通过实验证明小军的猜想成立.为进一步确定白色粉末中碳酸钠的质量分数,他们设计了如下2种不同的实验方案:
方案一:气体分析法--取2.5g白色粉末样品,放入锥形瓶(见下图),加入足量的盐酸充分反应,气体最后通入氢氧化钠溶液(假设气体全部被氢氧化钠吸收,忽略系统内空气中CO2的影响),两次称量盛氢氧化钠溶液的洗气瓶的质量,得前后两次质量差为0.90g.
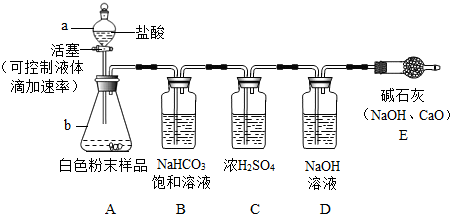
[实验讨论]
①向锥形瓶加入白色粉末样品前,必须进行的操作是 ;
②装置E的作用是 ;
③用B中NaHCO3饱和溶液除去CO2中混有的少量HCl气体,B中的NaHCO3溶液能否换成石灰水?请判断并写出理由 .
④老师和同学们都认为:不能根据以上实验数据0.90g计算白色粉末中碳酸钠的质量分数,理由是 ;
⑤为达到准确测定白色粉末样品中碳酸钠的质量分数的目的,应该加以改进,你认为改进方法是 .
方案二:沉淀分析法--另取一定量白色粉末的样品,按照下图所示的过程进行实验,测定产生的硅酸的质量以推算碳酸钠的质量分数.
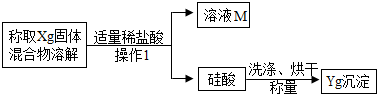
(1)“操作1”的名称是 _;
(2)确定盐酸是否适量的方法是 (说明实验的操作、现象与结论);
(3)若实验中所取样品的质量为3g,产生硅酸沉淀的质量为0.39g.计算该白色粉末中碳酸钠的质量分数.
[反思评价]导致测定的结果偏大的原因可能是 .
查看习题详情和答案>>
[提出问题]盛放NaOH溶液的试剂瓶瓶口的白色粉末究竟是什么物质?
[查阅资料](1)已知玻璃的主要成分是二氧化硅(Si02),它具能与CO2、SO2相似的化学性质,与氢氧化钠反应产生的硅酸钠(Na2SiO3)和水,硅酸钠也是一种白色固体,俗称“水玻璃”,它是一种凝胶,能将玻璃粘结在一起;
(2)硅酸钠和盐酸或硫酸能发生复分解反应,产生的硅酸(H2SiO3)是一种白色难溶解于水的固体.
[成分分析]同学们依据所学的化学知识结合从资料中获取的信息,对这种白色粉末的成分作了如下猜想:
①小军可能是Na2CO3和Na2SiO3的混合物;
②小红可能是NaOH、Na2CO3和Na2SiO3的混合物.
[实验验证]为了验证猜想,小红同学取少量上述白色粉末并完全溶于水,用pH试纸测得溶液的pH大于7,继续向溶液中滴加稀盐酸至过量,发现有气体生成,同时还有白色沉淀出现.由此小红认为自己的猜想成立.
(1)写出下列有关化学反应的化学方程式:
①二氧化硅(Si02)和氢氧化钠溶液的反应
②小红的实验中,白色沉淀形成的化学反应
[问题解答]
(2)实验室里不同化学试剂的保存方法不尽相同.现有①NaOH溶液、②硝酸银溶液、③大理石、④白磷、⑤稀硫酸等5种药品可分别保存在下列各试剂瓶中,请把NaOH溶液和硝酸银溶液的序号填写在各试剂瓶下面的括号内:
| A | B | C | D | E |
 |
 |
 |
 |
 |
| ( ) | ( ) | ( ) | ( ) | ( ) |
[含量测定]在老师的指导下,同学们设计了实验并通过实验证明小军的猜想成立.为进一步确定白色粉末中碳酸钠的质量分数,他们设计了如下2种不同的实验方案:
方案一:气体分析法--取2.5g白色粉末样品,放入锥形瓶(见下图),加入足量的盐酸充分反应,气体最后通入氢氧化钠溶液(假设气体全部被氢氧化钠吸收,忽略系统内空气中CO2的影响),两次称量盛氢氧化钠溶液的洗气瓶的质量,得前后两次质量差为0.90g.

[实验讨论]
①向锥形瓶加入白色粉末样品前,必须进行的操作是
②装置E的作用是
③用B中NaHCO3饱和溶液除去CO2中混有的少量HCl气体,B中的NaHCO3溶液能否换成石灰水?请判断并写出理由
④老师和同学们都认为:不能根据以上实验数据0.90g计算白色粉末中碳酸钠的质量分数,理由是
⑤为达到准确测定白色粉末样品中碳酸钠的质量分数的目的,应该加以改进,你认为改进方法是
方案二:沉淀分析法--另取一定量白色粉末的样品,按照下图所示的过程进行实验,测定产生的硅酸的质量以推算碳酸钠的质量分数.

(1)“操作1”的名称是
(2)确定盐酸是否适量的方法是
(3)若实验中所取样品的质量为3g,产生硅酸沉淀的质量为0.39g.计算该白色粉末中碳酸钠的质量分数.
[反思评价]导致测定的结果偏大的原因可能是
 生成知识是高效学习的一种体现.
生成知识是高效学习的一种体现.(1)发掘下面表格中隐含信息,并解决相关问题:
| 元素 | Na | Mg | Cl | S |
| 离子 | Na+ | Mg2+ | Cl- | S2- |
| 化合价 | +1 | +2 | -1 | -2 |
原子结构示意图 |
 |
 |
 |
 |
得几个电子,带几个单位负电荷,显负几价,失去几个电子,带几个单位正电荷,显正几价
得几个电子,带几个单位负电荷,显负几价,失去几个电子,带几个单位正电荷,显正几价
.②a.碳酸锂可以治疗燥狂病,它是由Li+和CO32-两种离子组成的化合物,它的化学式可以表示为
Li2CO3
Li2CO3
.b.纳米技术研究是当前世界科技研究的一个热点,1998年中国科学家合成了纳米氮化镓,已知氮和镓(Ga)的原子的结构示意图分别如图(1)(2)所示,则氮化镓的化学式为
GaN
GaN
.(2)甲烷是最简单的有机物,将来我们会在高中继续学习一些组成类似的物质,如下:
| 名称 | 甲烷 | 乙烷 | 丙烷 | … | 十五烷 | … |
| 化学式 | CH4 | C2H6 | C3H8 | C15H32 | … |
2x+2
2x+2
.②打火机的燃料是丁烷,它在空气中完全燃烧的产物跟甲烷相同,请你写出丁烷燃烧的化学方程式:
2C4H10+13O2
8CO2+10H2O
| ||
2C4H10+13O2
8CO2+10H2O
.
| ||