网址:http://m.1010jiajiao.com/timu_id_884214[举报]
【猜想与假设】
第一种:草酸分解产物CO2和H2
第二种:草酸分解产物是CO2、CO和H2O
第三种:草酸的分解产物是
【设计实验装置】
【实验】
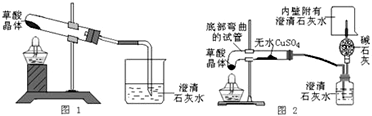
甲同学按其设计的实验装置(如图1)实验时观察到澄清的石灰水变浑浊了…;
乙同学按图2的装置实验也观察到澄清的石灰水变浑浊了,这些现象证明产物中一定有
| ||
| ||
【结论】
若第二种猜想是正确的,请你写出草酸分解的反应方程式
| ||
| ||
【反思与评价】
(1)乙认为甲设计的实验装置有缺陷:由于试管口向下倾斜,草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中会出现熔融的草酸流进导管而影响后续实验.请你谈谈装置2的至少两点优于装置1的优点:
(2)利用乙设计的装置证明产物中没有H2的方法是:
草酸的化学式为H2C2O4,甲、乙两位同学对草酸受热分解及其产物的检验分别做了探究:
【猜想与假设】
第一种:草酸分解产物CO2和H2
第二种:草酸分解产物是CO2、CO和H2O
第三种:草酸的分解产物是______(你猜想的产物化学式)
【设计实验装置】

【实验】
甲同学按其设计的实验装置(如图1)实验时观察到澄清的石灰水变浑浊了…;
乙同学按图2的装置实验也观察到澄清的石灰水变浑浊了,这些现象证明产物中一定有______; 无水CuSO4变蓝,证明产物中还有______;若产物中有CO,则乙的对应实验现象是______;证明CO生成的化学反应方程式是______.
【结论】
若第二种猜想是正确的,请你写出草酸分解的反应方程式______.
【反思与评价】
(1)乙认为甲设计的实验装置有缺陷:由于试管口向下倾斜,草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中会出现熔融的草酸流进导管而影响后续实验.请你谈谈装置2的至少两点优于装置1的优点:____________.
(2)利用乙设计的装置证明产物中没有H2的方法是:______.
查看习题详情和答案>>
【猜想与假设】
第一种:草酸分解产物CO2和H2
第二种:草酸分解产物是CO2、CO和H2O
第三种:草酸的分解产物是______(你猜想的产物化学式)
【设计实验装置】
【实验】
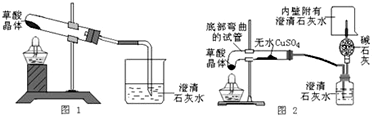
甲同学按其设计的实验装置(如图1)实验时观察到澄清的石灰水变浑浊了…;
乙同学按图2的装置实验也观察到澄清的石灰水变浑浊了,这些现象证明产物中一定有______; 无水CuSO4变蓝,证明产物中还有______;若产物中有CO,则乙的对应实验现象是______;证明CO生成的化学反应方程式是______.
【结论】
若第二种猜想是正确的,请你写出草酸分解的反应方程式______.
【反思与评价】
(1)乙认为甲设计的实验装置有缺陷:由于试管口向下倾斜,草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中会出现熔融的草酸流进导管而影响后续实验.请你谈谈装置2的至少两点优于装置1的优点:____________.
(2)利用乙设计的装置证明产物中没有H2的方法是:______.
草酸的化学式为H2C2O4,甲、乙两位同学对草酸受热分解及其产物的检验分别做了探究:
(1).[猜想与假设]
第一种:草酸分解产物CO2和H2
第二种:草酸分解产物是CO2、CO和H2O
第三种:草酸的分解产物是 、 (你猜想的产物化学式)
(2).[设计实验装置]
 |
(3).[实验]
甲同学按其设计的实验装置(如图1)实验时观察到澄清的石灰水变浑浊了...
乙同学按图2的装置实验也观察到澄清的石灰水变浑浊了,这些现象证明产物中一定有 ; 无水CuSO4变蓝,证明产物中还有
若产物中有CO,则乙的对应实验现象是
证明CO生成的化学反应方程式是
(4).[结论]若第二种猜想是正确的,请你写出草酸分解的反应方程式
。
(5).反思与评价]
乙认为甲设计的实验装置有缺陷:由于试管口向下倾斜,草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中会出现熔融的草酸流进导管而影响后续实验。请你谈谈装置2的至少两点优于装置1的优点:
。
利用乙设计的装置证明产物中没有H2的方法是:
查看习题详情和答案>>
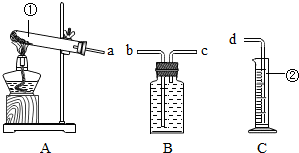 某校化学兴趣小组的同学利用下列装置进行实验.
某校化学兴趣小组的同学利用下列装置进行实验.【实验目的】:
一.用高锰酸钾制取一瓶氧气,做细铁丝燃烧的实验.
二.粗略测定加热2g高锰酸钾所收集到的氧气体积.
【反应原理】:(用化学式表达式表示)
高锰酸钾制氧气:
细铁丝在氧气中燃烧:
【装置连接】:
写出标数字的仪器名称:①
为达到实验二的目的,各装置的正确连接顺序是:(填接口的字母)a→
【问题分析】:
(1)实验过程发现B瓶中的水变红了,原因是:
(2)用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作可能是:
(3)在本实验中,收集氧气的时机是加热后马上收集,若是在气体连续不断产生之后才开始 收集,则测得的氧气的体积会比实际值
(4)实验结束时,乙同学发现收集到的氧气大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】
猜想I:反应生成的二氧化锰分解放出氧气;
猜想Ⅱ:反应生成的锰酸钾分解放出氧气.
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的二氧化锰装入试管,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变.则猜想
②第二组同学取锰酸钾装入试管,在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是