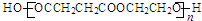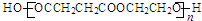摘要:(1)钠 . 3 .ⅡA . (4)2F2+2H2Oㄔ4HF+O2 (5)He (6)NaOH HF 3+OH-ㄔAlO-2+2H2O
网址:http://m.1010jiajiao.com/timu_id_85079[举报]
取一小块钠,刚切开时,断面呈
其反应的离子方程式为
 (标出电子转移的方向与数目):
(标出电子转移的方向与数目):
查看习题详情和答案>>
银白
银白
色,在空气中放置片刻,断面变暗
暗
,这是因为主要生成了氧化钠
氧化钠
.另取一小块钠,将其投入滴有酚酞的一烧杯水中,观察到的现象及结论为:(填写下表)| 现象(至少四个) | 结论 |
| 1.金属钠浮在水面上. 2.熔成小球. 3.小球四处游动,发出嘶嘶声. 4.溶液变成红色 5.Na消失 1.金属钠浮在水面上. 2.熔成小球. 3.小球四处游动,发出嘶嘶声. 4.溶液变成红色 5.Na消失 |
1钠的密度小于水; 2.Na的熔点低,反应放热; 3.生成H2 4.生成NaOH 1钠的密度小于水; 2.Na的熔点低,反应放热; 3.生成H2 4.生成NaOH |


 已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法:
已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法:★还原法:在酸性介质中用FeSO4等将+6价铬还原成+3价铬.
具体流程如下:

有关离子完全沉淀的pH如下表:
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
| O | 2- 7 |
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
.(2)还原+6价铬还可选用以下的
BD
BD
试剂(填序号).A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.则在操作②中可用于调节溶液pH的试剂为
CD
CD
(填序号).A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH在
B
B
(填序号)范围最佳.A.3~4 B.6~8 C.10~11 D.12~14
★电解法:将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2
| O | 2- 7 |
(4)写出阴极的电极反应式
2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-
2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-
.(5)电解法中加入氯化钠的作用是
增强溶液导电性或盐析
增强溶液导电性或盐析
.(6)若外接电源为熔融碳酸盐燃料电池,其工作原理示意图如图,则熔融碳酸盐燃料电池的正极反应可表示为
O2+4e-+2CO2═2CO32-
O2+4e-+2CO2═2CO32-
.高铁酸钾(K2FeO4)是铁的一种重要化合物,具有极强的氧化性.
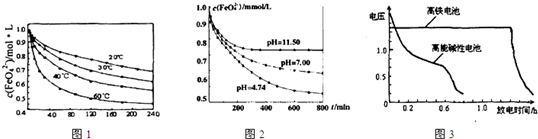
(1)将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO42-)=1.0×10-3mol?L-的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)随时间变化的结果如图1所示.
该实验的目的是
(2)将适量K2FeO4分别溶解于pH=4.74、7.00、11.50的水溶液中,配制成c(FeO42-)=1.0×10-3 mol?L-的试样,静置,考察不同初始pH的水溶液对K2FeO4某种性质的影响,其变化图象见图2,800min时,在pH=11.50的溶液中,K2FeO4的浓度比在pH=4.74的溶液中高,主要原因是
(3)电解法是工业上制备K2FeO4的一种方法.以铁为阳极电解氢氧化钠溶液,然后在阳极溶液中加入KOH,即在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明
(4)与MnO2-Zn电池类似,K2FeO4-Zn也可以组成高铁电池,K2FeO4在电池中作正极材料,其电极反应式为FeO42-+3eˉ+4H2O→Fe(OH)3+5OHˉ,则该电池总反应的离子方程式为
查看习题详情和答案>>

(1)将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO42-)=1.0×10-3mol?L-的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)随时间变化的结果如图1所示.
该实验的目的是
探究温度对FeO42-影响(温度越高,高铁酸钾越不稳定)
探究温度对FeO42-影响(温度越高,高铁酸钾越不稳定)
;FeO42-发生反应的△H>
>
0(填“>”“<”或“=”)(2)将适量K2FeO4分别溶解于pH=4.74、7.00、11.50的水溶液中,配制成c(FeO42-)=1.0×10-3 mol?L-的试样,静置,考察不同初始pH的水溶液对K2FeO4某种性质的影响,其变化图象见图2,800min时,在pH=11.50的溶液中,K2FeO4的浓度比在pH=4.74的溶液中高,主要原因是
pH=11.50时溶液中OHˉ离子浓度大,不利于K2FeO4与水的反应正向进行
pH=11.50时溶液中OHˉ离子浓度大,不利于K2FeO4与水的反应正向进行
.(3)电解法是工业上制备K2FeO4的一种方法.以铁为阳极电解氢氧化钠溶液,然后在阳极溶液中加入KOH,即在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明
同温度下,高铁酸钾的溶解度比高铁酸钠的溶解度小
同温度下,高铁酸钾的溶解度比高铁酸钠的溶解度小
.电解时阳极发生反应生成FeO42-,该电极反应式为Fe+8OHˉ-6eˉ=FeO42-+4H2O
Fe+8OHˉ-6eˉ=FeO42-+4H2O
.(4)与MnO2-Zn电池类似,K2FeO4-Zn也可以组成高铁电池,K2FeO4在电池中作正极材料,其电极反应式为FeO42-+3eˉ+4H2O→Fe(OH)3+5OHˉ,则该电池总反应的离子方程式为
3Zn+2FeO42-+8H2O=3Zn(OH)2+2Fe(OH)3+4OHˉ
3Zn+2FeO42-+8H2O=3Zn(OH)2+2Fe(OH)3+4OHˉ
.如图3为高铁酸钾电池和高能碱性电池放电曲线,由此可得出的高铁酸钾电池的优点有放电时间长
放电时间长
、工作电压稳定
工作电压稳定
.(2011?昌平区二模)铁元素及其化合物与人类的生产生活息息相关,回答下列问题
(1)铁酸钠(Na2FeO4)是一种新型水处理剂,它有比高锰酸钾更强的氧化性,在水中反应被还原为Fe3+.
①铁酸钠中铁元素的化合价为
②铁酸钠用于水处理,除了能消毒杀菌外,还可以像明矾(KAl(SO4)2)一样起到净水作用,请说明明矾的净水原理:
(2)反应ⅠFe(s)+CO2(g)?FeO(s)+CO(g)△H=a kJ?mol-1,平衡常数为K;
反应ⅡCO(g)+1/2O2(g)=CO2(g)△H=b kJ?mol-1测得在不同温度下,K值如下:
①写出反应Ⅰ的K的表达式
②反应Ⅰ中的a
③若500℃时进行反应Ⅰ,CO2起始浓度为2mol?L-1,CO的平衡浓度为
④700℃反应Ⅰ达到平衡,要使得该平衡向右移动,其它条件不变时,可以采取的措施有
A.缩小反应器体积 B.通入CO2
C.升高温度到900℃D.使用合适的催化剂
⑤由反应Ⅰ和Ⅱ可求得,反应2Fe(s)+O2(g)=2FeO(s)的△H=
(3)铁红是一种红色颜料,其成份是Fe2O3.将一定量的铁红溶于160mL 5mol?L-1盐酸中,再加入一定量铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为
查看习题详情和答案>>
(1)铁酸钠(Na2FeO4)是一种新型水处理剂,它有比高锰酸钾更强的氧化性,在水中反应被还原为Fe3+.
①铁酸钠中铁元素的化合价为
+6
+6
.②铁酸钠用于水处理,除了能消毒杀菌外,还可以像明矾(KAl(SO4)2)一样起到净水作用,请说明明矾的净水原理:
Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
.(用离子方程式表示)(2)反应ⅠFe(s)+CO2(g)?FeO(s)+CO(g)△H=a kJ?mol-1,平衡常数为K;
反应ⅡCO(g)+1/2O2(g)=CO2(g)△H=b kJ?mol-1测得在不同温度下,K值如下:
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
k=
| c(CO) |
| c(CO2) |
k=
.| c(CO) |
| c(CO2) |
②反应Ⅰ中的a
大于
大于
0(填大于、小于、等于).③若500℃时进行反应Ⅰ,CO2起始浓度为2mol?L-1,CO的平衡浓度为
1
1
mol?L-1.④700℃反应Ⅰ达到平衡,要使得该平衡向右移动,其它条件不变时,可以采取的措施有
BC
BC
(填序号).A.缩小反应器体积 B.通入CO2
C.升高温度到900℃D.使用合适的催化剂
⑤由反应Ⅰ和Ⅱ可求得,反应2Fe(s)+O2(g)=2FeO(s)的△H=
2(a+b)
2(a+b)
kJ?mol-1.(3)铁红是一种红色颜料,其成份是Fe2O3.将一定量的铁红溶于160mL 5mol?L-1盐酸中,再加入一定量铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为
11.2
11.2
g.(2011?南开区一模)有机化合物A~H的转换关系如下所示:
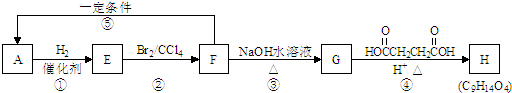
请回答下列问题:
(1)链烃A有支链且只有一个官能团,其相对分子质量在65~75之间,1mol A完全燃烧消耗7mol O2,则A的分子式为
(2)在特定催化剂作用下,A与等物质的量的H2反应生成E.由E转化为F的化学方程式是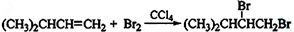
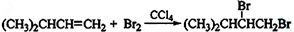 .
.
(3)G与金属钠反应能放出气体.G分子中所含官能团的名称是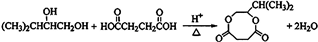
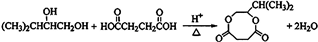 .
.
(4)①的反应类型是
(5)写出由F转化为A的反应条件是
(6)链烃B是A的同分异构体,分子中的所有碳原子共平面,其催化氢化产物为正戊烷,写出B所有可能的结构简式:
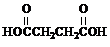
(7)丁二酸
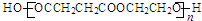
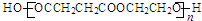 .
.
查看习题详情和答案>>

请回答下列问题:
(1)链烃A有支链且只有一个官能团,其相对分子质量在65~75之间,1mol A完全燃烧消耗7mol O2,则A的分子式为
C5H8
C5H8
,结构简式为(CH3)2CHC≡CH
(CH3)2CHC≡CH
,A的名称是3-甲基-1-丁炔
3-甲基-1-丁炔
.(2)在特定催化剂作用下,A与等物质的量的H2反应生成E.由E转化为F的化学方程式是
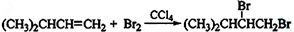
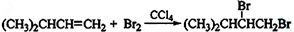
(3)G与金属钠反应能放出气体.G分子中所含官能团的名称是
羟基
羟基
;由G转化为H的化学方程式是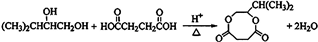
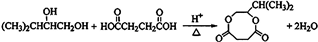
(4)①的反应类型是
加成反应
加成反应
;③的反应类型是水解反应
水解反应
.(5)写出由F转化为A的反应条件是
氢氧化钠醇溶液、加热
氢氧化钠醇溶液、加热
.(6)链烃B是A的同分异构体,分子中的所有碳原子共平面,其催化氢化产物为正戊烷,写出B所有可能的结构简式:
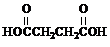
CH3CH=CHCH=CH2(或写它的顺、反异构体)、CH3CH2CHC≡CCH3
CH3CH=CHCH=CH2(或写它的顺、反异构体)、CH3CH2CHC≡CCH3
.(7)丁二酸
删除此空
删除此空
与乙二醇(HOCH2CH2OH)在催化剂作用下,经聚合反应可制成一种新型可生物降解的高分子材料.请写出该聚合物的结构简式: