网址:http://m.1010jiajiao.com/timu_id_76868[举报]
一、单项选择题(本题包括8小题,每题3分,共24分。)
1.C 2.C 3.D 4.A 5.A 6.D 7.B 8.B
二、不定项选择题(本题包括6小题,每小题4分,共24分。)
9.BD 10.A 11.D 12.BD 13.BC 14.D
三、非选择题(本题包括6小题,共60分)
15、(10分)
(1)Fe2+ (1分)
(2)4FeCO3+O22Fe2O3+4CO2 (2分) 坩埚、坩埚钳 (2分)
(3)K2SO4 (1分) 蒸发结晶、洗涤(2分)
(4)滴加过量Ba(NO3)2溶液,过滤后向滤液滴加AgNO3溶液。(2分)
16.(8分) ⑴Cu、O; ⑵b、c;
⑶2Fe3++2I-=2Fe2++I2;S2O82-+2Fe2+=2SO42-+2Fe3+;
⑷a: Al3++4OH-=AlO2-+2H2O[或Al3++4OH-=Al(OH)4-];
b:稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色
17、(12分)
(1)四 (1分) ⅥB (1分)
(2)① Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O (2分)
② Cr3+ + 4OH- = CrO2- + 2H2O (2分)
③ 8~10 (1分) ④ ABCD (2分)
(3)① 符合 (1分)
② (以下任意2条即可)(2分)
其它条件相同时,含铬废渣掺入的比例越大,Cr元素浸出的浓度越高;
酸性环境对Cr元素浸出有抑制作用;
冻融对Cr元素浸出影响不明显;或曝晒对Cr元素浸出影响不明显;
18、(10分)
(1)0.3 mol/(L?min) 升高温度
(2)
(3)-41.2 kJ/mol a
19、(12分)
(1)4
(2) 还原反应
(3)、
(4)
20.(10分)
⑴ ①
② 解:(C6H10O5)n~n C6H12O6~2nC2H5OH~nCH3COOC2H5
162n 88n
1000kg×90%×85%×90%×90% m(CH3COOC2H5)
m(CH3COOC2H5)=374 kg
⑵ 解:[(C6H7O2)(OH)3]n~[(C6H7O2)(OH)(3-x)(OOCCH3)x]n △m
162n 162n+42nx 42nx
10g 15.19g 5.19g
= x=2
故该醋酸纤维的结构简式为[(C6H7O2)(OH)(OOCCH3)2]n
四、选做题(本题包括1小题,共12分)
21.(12分)
A.⑴ O>N>C 1s22s22p63s23p63d84s2
⑵ 顺铂易溶于水,因为它是极性分子,易溶于极性溶剂
⑶ 4
⑷ ① ② sp3和sp2
 江苏省金湖中学2009届高三化学周练答题纸
江苏省金湖中学2009届高三化学周练答题纸
(本卷满分120分,考试时间100分钟)
第Ⅰ卷
选择题
1
2
3
4
5
6
7
8
9
10
11
12
13
14
――
――
――
――
非选择题
答题说明:除作图可使用2B铅笔外,其余各题请按题号用0.5mm黑色签字笔书写,否则作答无效。
非选择题(共72分)
15.(10分)
(1)酸浸、过滤后滤液中的金属阳离子是________________。
(2)化学反应方程式为____________________________。
_________、_________。
(3)产品Ⅱ的化学式为_______________,
操作是: __ 、趁热过滤、 __ 、干燥。
(4) ______
______________________________________________ 。
16.(8分)
(1) ( 填元素符号);
(2) (填代号)。
(3) 、
(不必配平);
(4)a.除去Al3+的离子方程式是 。
b.所选试剂为 。
实验现象为 。
请在各题规定的矩形区域内答题,超出该区域的答案无效!
17.(12分)
(1)第_______周期_______族。
(2)① 离子方程式为_________________________________________________。
② 离子方程式为_________________________________________________。
③ pH应控制在 范围内。
④ 说法中正确的是 。
(3)① 实验取用的砖样是否符合上述标准: 。
② 还能得出的其它结论是(写出2条即可):
_______________________________________________________________;
_______________________________________________________________。
18. (10分)
(1)v(H2)= 。 改变的外界条件可能是 。
(2)
(3) 。
19. (12分)
(1) 。 (2) ; 。
(3)、 、 。
(4)
请在各题规定的矩形区域内答题,超出该区域的答案无效!
20、(8分)
(1)①五元环结构为 。
②
(2)
四、选做题:
21、(12分)
(1)C、N、O三种元素的电负性由大到小的顺序是 ;
Ni元素基态原子的电子排布式: 。
(2)理由: 。
(3)含有 个铂原子。
(4)① 化合物X的结构式为 (必须标明配位键)。
② 化合物X、Y分子中,N元素分别发生了 杂化。
请在各题规定的矩形区域内答题,超出该区域的答案无效!
A.若温度不变,将容器体积增大一倍,此时A的浓度变为原来的0.48倍,则m+n>p+q??
B.若平衡时,A的转化率比B大,说明反应开始时,A与B的物质的量之比大于m∶n??
C.若m+n=p+q,则往含有a mol 气体的平衡体系中再加入b mo1 B,达到新平衡时,气体的总的物质的量等于(a+b)mol??
D.温度不变时,若压强增大至原来的2倍,达到新平衡时,总体积一定比原体积的![]() 要小
要小
|
对于平衡体系mA(g)+nB(g) | |
A. |
若平衡时 |
B. |
若温度不变,将容器的体积增大1倍,此时A的浓度变为原来的0.45倍,则m+n>p+q |
C. |
若m+n=p+q,则往含有amol气体的平衡体系中再加入bmolB,达到新平衡时,气体的总物质的量等于(a+b)mol |
D. |
若升高温度时,平衡混合气体的平均相对分子质量增大,则m+n>p+q |
(13分)合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g) 2NH3(g) △H= -92.4 kJ/mol 据此回答以下问题:
(1)合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是 (填序号)。
①反应压强为20Mpa~50Mpa ②500℃的高温 ③铁触媒作催化剂 ④将生成的氨液化并及时从体系中分离出来,未反应的N2、H2循环到合成塔中。
(2)一定条件下NH3的平衡体积分数随n(N2)变化如图所示(T-温度)。则T2 T1(填>、=、<),判断的依据是:
(3)合成氨气所需的氢气可以由水煤气分离得到。涉及反应信息如下:
反应一:C(s)+H2O(g) H2(g)+CO(g) 平衡常数K1
反应二:CO(g)+H2O(g) H2(g)+CO2(g) 平衡常数K2
① K1的表达式:K1=
②将一定量的H2O(g)和CO(g)分别通入到体积为1L的密闭容器中,在不同条件下进行反应,得到以下三组数据:
| 实验组别 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
| 2 | 900 | 0.5 | 1 | 0.2 | 0.8 | 3 |
| 3 | T | a | b | c | d | t |
(Ⅰ)实验1中,用CO2表示反应开始到平衡的平均反应速率为
(Ⅱ) 在实验3,当a=0.5、b=1时,要使c、d数据与实验2相同,且t<3,可以采取的措施为 (填序号)
A.其它条件不变温度T<900℃ B.其它条件不变温度T>900℃
C.充入一定量氖气 D.使用高效催化剂
(Ⅲ)对于反应二,当升高温度时K2 (填“增大”、“减小”或“不变”)。
查看习题详情和答案>>
(13分)合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g)  2NH3(g) △H=" -92.4" kJ/mol 据此回答以下问题:
2NH3(g) △H=" -92.4" kJ/mol 据此回答以下问题:
(1)合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是 (填序号)。
①反应压强为20Mpa~50Mpa ②500℃的高温 ③铁触媒作催化剂 ④将生成的氨液化并及时从体系中分离出来,未反应的N2、H2循环到合成塔中。
(2)一定条件下NH3的平衡体积分数随n(N2)变化如图所示(T-温度)。则T2 T1(填>、=、<),判断的依据是: 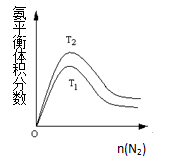
(3)合成氨气所需的氢气可以由水煤气分离得到。涉及反应信息如下:
反应一:C(s)+H2O(g)  H2(g)+CO(g) 平衡常数K1
H2(g)+CO(g) 平衡常数K1
反应二:CO(g)+H2O(g)  H2(g)+CO2(g) 平衡常数K2
H2(g)+CO2(g) 平衡常数K2
① K1的表达式:K1=
②将一定量的H2O(g)和CO(g)分别通入到体积为1L的密闭容器中,在不同条件下进行反应,得到以下三组数据:
| 实验组别 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
| 2 | 900 | 0.5 | 1 | 0.2 | 0.8 | 3 |
| 3 | T | a | b | c | d | t |
(Ⅱ)在实验3,当a=0.5、b=1时,要使c、d数据与实验2相同,且t<3,可以采取的措施为 (填序号)
A.其它条件不变温度T<900℃ B.其它条件不变温度T>900℃
C.充入一定量氖气 D.使用高效催化剂
(Ⅲ)对于反应二,当升高温度时K2 (填“增大”、“减小”或“不变”)。 查看习题详情和答案>>
(13分)合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g)  2NH3(g) △H= -92.4 kJ/mol 据此回答以下问题:
2NH3(g) △H= -92.4 kJ/mol 据此回答以下问题:
(1)合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是 (填序号)。
①反应压强为20Mpa~50Mpa ②500℃的高温 ③铁触媒作催化剂 ④将生成的氨液化并及时从体系中分离出来,未反应的N2、H2循环到合成塔中。
(2)一定条件下NH3的平衡体积分数随n(N2)变化如图所示(T-温度)。则T2 T1(填>、=、<),判断的依据是:

(3)合成氨气所需的氢气可以由水煤气分离得到。涉及反应信息如下:
反应一:C(s)+H2O(g)  H2(g)+CO(g)
平衡常数K1
H2(g)+CO(g)
平衡常数K1
反应二:CO(g)+H2O(g)  H2(g)+CO2(g) 平衡常数K2
H2(g)+CO2(g) 平衡常数K2
① K1的表达式:K1=
②将一定量的H2O(g)和CO(g)分别通入到体积为1L的密闭容器中,在不同条件下进行反应,得到以下三组数据:
|
实验组别 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
||
|
H2O |
CO |
H2 |
CO |
|||
|
1 |
650 |
1 |
2 |
0.8 |
1.2 |
5 |
|
2 |
900 |
0.5 |
1 |
0.2 |
0.8 |
3 |
|
3 |
T |
a |
b |
c |
d |
t |
(Ⅰ)实验1中,用CO2表示反应开始到平衡的平均反应速率为
(Ⅱ) 在实验3,当a=0.5、b=1时,要使c、d数据与实验2相同,且t<3,可以采取的措施为 (填序号)
A.其它条件不变温度T<900℃ B.其它条件不变温度T>900℃
C.充入一定量氖气 D.使用高效催化剂
(Ⅲ)对于反应二,当升高温度时K2 (填“增大”、“减小”或“不变”)。
查看习题详情和答案>>