网址:http://m.1010jiajiao.com/timu_id_67373[举报]
一. 选择题:(3分×16=48分)
题 号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答 案
D
C
A
A
C
D
A
D
C
B
D
D
B
A
C
C
二.(本题共14分)
17:Ⅰ.(4分,每空1分)(1)AEF;(2)BDE ;AF;(3)F>A>C>B>E。
Ⅱ.(10分)本题答案有开放性,合理即可给分。
⑴①C(或Fe) (1分) ②
⑵CuO(Fe2O3等)(1分)
⑶①CaC2+2H2O=Ca(OH)2+C2H2↑ ;(2分) ②麦芽糖;(1分)
⑷①Na2CO3+CO2+H2O=2NaHCO3 ;(2分) ②红褐色固体。(1分)
三.(本题共20分)
18.(10分)(1)高氯酸 (1分) (2)离子键和非极性键 (1分)
(3)2I-+ClO-+H2O=I2+Cl-+2OH- (2分)
(4)2H++2e- = H2↑ (2分) 0.71g (2分)
(5)2H2(g)+O2(g)=2H2O(g) ΔH=-4QkJ/mol (2分)
19.(10分)
(1)③④⑥(2分) (2)Ca(OH)2 或 Ba(OH)2(2分)
(3)2Na + 2H2O = 2Na++ 2OH- + H2↑(2分)
(4)氧化还原:2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑ (2分)
非氧化还原:AlCl3 + 4NaOH = NaAlO2 +3NaCl +2H2O (2分)
或Al(OH)3 + NaOH = NaAlO2 + 2H2O
或Al2O3 + 2NaOH = 2NaAlO2 + H2O
(其它合理答案酌情给分)
四. (本题共9分) (每空1分)
20.Ⅰ(1)关闭分液漏斗的活塞,在B中加水至浸没长导管口,用酒精灯微热(或用手热),长导管口有气泡冒出,停止加热,长导管内形成一段水柱,说明装置的气密性良好。
(2)圆底烧瓶; 常温下,Fe在浓硫酸中钝化,碳不与浓硫酸反应
(3)C+2H2SO4(浓) CO2↑+2SO2↑+2H2O; 品红溶液逐渐褪色
CO2↑+2SO2↑+2H2O; 品红溶液逐渐褪色
(4)2Fe3++Fe=3Fe2+(或Fe+2H+=Fe2++H2↑)
(5)铁碳在酸溶液中形成原电池
Ⅱ(6) (7)C
(7)C
五.(本题共9分) 21.
如图,有甲、乙两容器,甲体积可变压强不变,乙保持体积不变。向两容器中分别充人lmdA、3molB,此时两容器体积均为500mL,温度为T0C保持温度不变发生反应:
(1) 下列选项中,能表明甲和乙容器中反应一定达到平衡状态的是__ __ (2分,全才得分)。
A.混合气体的总质量不随时间改变 B 2V正 (C)=3V逆(B)
C. A、B转化率相等 D.物质D的质量不随时间改变
(2) 2minn后甲容器中反应达到平衡,测得C的浓度为2mol/L,此时容器的体积为____(2分)mL,B的转
化率a甲(B)为____ (2分)。
(3) 乙容器中反应达到平衡所需要的时间____2min(2分)(填“>”、“<”或“=”,下同),B的转化率a乙(B)为___ a甲(B) (2分)。
(4) 其它条件不变,甲中如果从逆反应方向开始建立平衡,要求平衡时C的物质的量与(2)中平衡时C的物质的量相等,则需要加人C的物质的量n(C)为____ (2分)mol,加人D的物质的量n(D)应该满足的条件为 (2分)。
查看习题详情和答案>>
如图,有甲、乙两容器,甲体积可变压强不变,乙保持体积不变。向两容器中分别充人lmdA、3molB,此时两容器体积均为500mL,温度为T0C保持温度不变发生反应:


(1) 下列选项中,能表明甲和乙容器中反应一定达到平衡状态的是__ __ (2分,全才得分)。
A.混合气体的总质量不随时间改变 B 2V正 (C)=3V逆(B)
C. A、B转化率相等 D.物质D的质量不随时间改变
(2) 2minn后甲容器中反应达到平衡,测得C的浓度为2mol/L,此时容器的体积为____(2分)mL,B的转
化率a甲(B)为____ (2分)。
(3) 乙容器中反应达到平衡所需要的时间____2min(2分)(填“>”、“<”或“=”,下同),B的转化率a乙(B)为___ a甲(B) (2分)。
(4) 其它条件不变,甲中如果从逆反应方向开始建立平衡,要求平衡时C的物质的量与(2)中平衡时C的物质的量相等,则需要加人C的物质的量n(C)为____ (2分)mol,加人D的物质的量n(D)应该满足的条件为 (2分)。
查看习题详情和答案>>
(8分)有效地利用现有新能源和开发新能源已受到各国的重视。
(1)工业上可用改进汽油组成的办法来改善汽油的燃烧性能。例如,加入CH30C(CH3)3,来生产无铅汽油”。 H3COC(CH3)3分子必存在的原子间连接形式有 。(填写编号,多选不得分)
①>C=0 ②>C=C< ③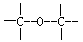 ④
④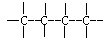
(2)天然气的燃烧产物无毒、热值高、管道输送方便,将成为我国西部开发的重点之一,天然气常和石油伴生,其主要的成分是甲烷。能说明它是正四面体而非正方形平面结构的理由是 。(填写编号)
①其一氯取代物不存在同分异构体 ②其二氯取代物不存在同分异构体
(3)1980年我国首次制成一辆燃氢汽车,乘员12人,以50km/h行驶了40km。为了有效发展民用氢能源,首先必须制得廉价的氢气。下列可供开发又较经济的制氢方法是
①电解水 ②锌和稀硫酸反应 ③光解海水
(4)其次,制得纯氢气后,还需要解决的问题是 。(写出其中的一个)
(8分)有效地利用现有新能源和开发新能源已受到各国的重视。
(1)工业上可用改进汽油组成的办法来改善汽油的燃烧性能。例如,加入CH30C(CH3)3,来生产无铅汽油”。 H3COC(CH3)3分子必存在的原子间连接形式有 。(填写编号,多选不得分)
①>C=0
②>C=C< ③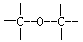 ④
④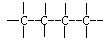
(2)天然气的燃烧产物无毒、热值高、管道输送方便,将成为我国西部开发的重点之一,天然气常和石油伴生,其主要的成分是甲烷。能说明它是正四面体而非正方形平面结构的理由是 。(填写编号)
①其一氯取代物不存在同分异构体 ②其二氯取代物不存在同分异构体
(3)1980年我国首次制成一辆燃氢汽车,乘员12人,以50km/h行驶了40km。为了有效发展民用氢能源,首先必须制得廉价的氢气。下列可供开发又较经济的制氢方法是
①电解水 ②锌和稀硫酸反应 ③光解海水
(4)其次,制得纯氢气后,还需要解决的问题是 。(写出其中的一个)
查看习题详情和答案>>
(26分)
⑴棉花纤维的化学成分是 。大豆油的主要成分是 。蚕丝和羊毛的化学成分是 。如何区分棉纤维和羊毛?
⑵一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收。
1) 在人体中进行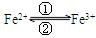 的转化时,①中的Fe2+作 剂;②中的Fe3+作 剂
的转化时,①中的Fe2+作 剂;②中的Fe3+作 剂
2) “服用维生素C,可使食物中的Fe3+ 还原成Fe2+”这句话指出,维生素C在这一反应中作 剂,具有 性;
3) 市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐。此反应的离子方程式为 。
⑶汽车已经成为重要的交通工具,但其排放的尾气是空气的主要污染物之一。已知汽车尾气中的主要污染物有:CmHn(烃)、SO2、NOX、CO和C等,请回答下列有关问题。
1)若用CmHn表示汽油的主要组成,CmHn在空气中完全燃烧的化学方程式为 ,汽油燃烧产生能量为汽车提供了动力,这一过程中能量的转化是由 能转化为热能,最终转化为机械能;
2)通过车用燃油的精炼加工处理,可减少汽车尾气中的 (填化学式,多填本空不得分)排放;
3)目前汽车尾气多采用催化转化的方法加以治理,写出在催化剂作用下NOX与CO反应的化学方程式 。