网址:http://m.1010jiajiao.com/timu_id_6661[举报]
(一)选择题
1.C 2.A、C 3.D 4.C 5.B、D 6.A 7.C 8.A、D 9.C 10.B 11.A
(二)非选择题
1.(1)过滤;蒸发 (2)B (3)滤液浑浊 (4)液体飞溅 (5)K2CO3,KCl,K2SO4
2.(1)先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和冷却 (2)将反应容器 放在50~60℃的水浴中加热 (3)分液漏斗 (4)除去粗产品中的残留酸 (5)大,苦杏仁
3.(1)除去吸入空气中的CO2 (2)D (3)可增大气体与溶液的接触面,使气体中的CO2被充分吸收;
(4)
(5)把瓶Ⅰ中的NaOH溶液吸入口中;把瓶Ⅱ中的NaOH溶液吹出瓶外
4.(1)增加一种反应物,有利于酯化反应向正反方向进行 (2)蒸出生成物,有利于酯化 反应向正反应方向进行 (3)B (4)除去粗产品中的乙醇 (5)除去粗产品中的水
5.(1)①适当稀释浓H2SO4,防止HBr被氧化 ②吸收溶解的HBr。
(2)②控制恒温,38.4℃。该温度下只有溴乙烷蒸馏出来。
(3)②使沸点高于溴乙烷的副产品回流。
(4)及时分馏出产物,促使平衡正向移动。
(5)密度比水大且难溶于水,水封,防止蒸气逸出,并防止倒吸,E。
6.(1)Ⅱ (2)F,G,E,H 吸收空气中的水蒸气和CO2 (3)F,C (4)A,B,C,F
(5)C2H5OH+CuOCH3CHO+Cu+H2O 乙醛,乙醇 (6)E,G 不合理
7.(1)b,c,a,c,d 吸收未反应的氨,防止空气水分进入 ② 固体由黑色变为红色;③a,c (2)a,c
8.(1)A,B,D,F,G,H,J 坩锅 泥三角 药匙 (2)(W2-W3)/(W2-W1)×100% 偏高 A,D
9.(1)使Fe2+氧化成易于分离的Fe3+
(2)A (3)CuO,Fe(OH)3和过量的CuO
(4)A,B,D,G,I
10.(1)是由于氯水中氢离子与碱中和 (2)是氯水中次氯酸氧化所致。
11.(1)过滤,萃取,Cl2+2I-=I2+2Cl-
(2)B (3)分液漏斗
(4)①缺石棉网 ②温度计插到了液体中 ③冷凝管进出水的方向颠倒
(5)使蒸馏烧瓶受热均匀,控制温度,以防止碘在局部高温时升华。蒸馏烧瓶
12.(1)32g/mol N2H4 (2)N2H4+2CuO2Cu+N2+2H2O
13.(1)把导管b的下端浸于水中,用手握紧试管a,导管会有气泡冒出;松开后,水又会回升到导管b中。 (2)3Cu+8HNO33Cu(NO3)2+2NO↑+4H2O 2NO+O2=2NO2
(3)①铜片上有无色气泡产生,反应速率开始缓慢,后逐渐加快;②试管上部空间由无色变为浅棕色,又变成无色;③试管a中的溶液由无色变为浅蓝色;④反应结束时,铜片全部溶解。(4)由于反应开始时产生的NO和试管a上部空气中的O2作用生成NO2,N O2易溶于水并与水反应,使度管a内气体压强暂时减小,所以导管中的水面会上升到一定 高度
(5)①水进入试管,上升到一定高度;②试管中气体的颜色由棕色变为无色。
14.(1)红棕色 (2)溴与AgNO3反应生成AgBr沉淀,无法确定溴与苯反应有HBr生成
(3 )①吸收烧瓶中的溴蒸气,减少对环境污染 ②与混合液中残余的溴反应,以利于溴苯的提纯 、分离
15.(1)B (2)把该仪器放入冰水里,玻璃管内混合气体颜色变浅;或把该仪器放入热水里, 玻璃管内混合气体颜色变深
16.(1)①c ②a ③检查装置的气密性 本反应为放热反应 ④将系统内的空气排尽 c
(2)①干燥气体 ②使两种气体充分混合 ③观察气泡以调节氢、氮气流速度
NH3及N2、H2的混合物 用蘸有浓盐酸的玻璃棒放在导管口,有白烟说明有氨生成
17.①A,B ②[K+]≥0.2mol/L []=0.1mol/L [] =0.2mol/L
[]=0.4mol/L
18.(1)NaOH、BaCl2、Na2CO3、HCl
(2)2NaCl+2H2O2NaOH+2H2+2Cl2?
(3)干燥的HCl,防止MgCl2?6H2O受热脱水时水解。
aE,C, NaCl+H2SO4(浓) NaHSO4+HCl?
bL⑤、①、②、③、⑦、④、③
cM浓H2S4,稀NaOH,NaCl(s),MgCl2?6H2O,浓H2SO4
d吸收HCl气体,白色酸雾。
19.(1)SOCl2+H2O2HCl+SO2↑
(2)由SOCl2与水反应“剧烈”,可知SOCl2与晶体ZnCl2?3H2O混合共热时,SOCl2就优先于Zn2+与水结合,生成HCl,因而从两个方面抑制ZnCl2水解:
ZnCl2+H2OZn(OH)Cl+HCl,得到无水ZnCl2。
(3)C2H5OH+SOCl2C2H5Cl+SO2↑+HCl↑
(4)由题给信息可知SOCl2的沸点仅为77℃,较低,所以可用蒸馏的方法除去。故选D。
下图所示装置进行有关实验,将A逐滴加入B中
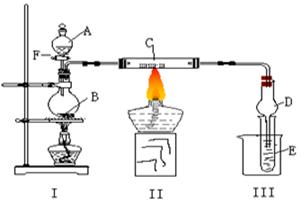
⑴若A是实验室的一种常用燃料,B是生石灰,实验中观察到C中黑色固体逐渐变红,当C中黑色固体大部分变红时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁出现了光亮的银镜,则A是 ,C是 ,请写出反应管C中所发生的反应方程式: 。 试管E中所发生反应的离子方程式: 。
⑵若I处酒精灯不加热, B、C仍是实验(1)中原物质,实验中也观察到C中黑色固体逐渐变红,同时可观察到E中溶液先形成沉淀,然后沉淀溶解,并有一种无色无味的气体逸出,当溶液恰好澄清时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁也出现了光亮的银镜,则A是 ,E中是 与葡萄糖的混合液(写化学式)。请写出反应管C中所发生反应的方程式: 。仪器D在此实验中的作用是 。
⑶若B为浓硫酸,E为苯酚钠溶液,C仍旧不变,A是只含一个碳的一种有机物也能发生银镜反应,实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管中溶液变浑浊,则A可能是 ,然后往烧杯中加入沸水,可观察到试管中的现象是 ,此实验中浓硫酸的作用是 。写出(1)中A和(3)中A二种物质在浓硫酸存在时所发生的反应方程式: ,此反应中浓硫酸的作用是 。
查看习题详情和答案>>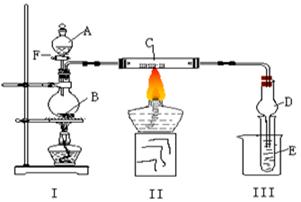
⑴若A是实验室的一种常用燃料,B是生石灰,实验中观察到C中黑色固体逐渐变红,当C中黑色固体大部分变红时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁出现了光亮的银镜,则A是 ,C是 ,请写出反应管C中所发生的反应方程式: 。试管E中所发生反应的离子方程式: 。
⑵若I处酒精灯不加热, B、C仍是实验(1)中原物质,实验中也观察到C中黑色固体逐渐变红,同时可观察到E中溶液先形成沉淀,然后沉淀溶解,并有一种无色无味的气体逸出,当溶液恰好澄清时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁也出现了光亮的银镜,则A是 ,E中是 与葡萄糖的混合液(写化学式)。请写出反应管C中所发生反应的方程式: 。仪器D在此实验中的作用是 。
⑶若B为浓硫酸,E为苯酚钠溶液,C仍旧不变,A是只含一个碳的一种有机物也能发生银镜反应,实验中同样能观察到C中黑色固体逐渐变红,同时可观察到试管中溶液变浑浊,则A可能是 ,然后往烧杯中加入沸水,可观察到试管中的现象是 ,此实验中浓硫酸的作用是 。写出(1)中A和(3)中A二种物质在浓硫酸存在时所发生的反应方程式: ,此反应中浓硫酸的作用是 。
实验室制硝基苯的主要步骤如下:
 ① 在250mL的圆底烧瓶中放入17.7 mL苯,配上一个双孔橡皮塞,一个孔插入一支100℃温度计,其水银球要进入液面下,另一个孔插入长颈漏斗,仪器装置如图所示。
① 在250mL的圆底烧瓶中放入17.7 mL苯,配上一个双孔橡皮塞,一个孔插入一支100℃温度计,其水银球要进入液面下,另一个孔插入长颈漏斗,仪器装置如图所示。
②通过长颈漏斗上口将已配制好的混酸分多次加入烧瓶中。每加一次,必须振荡烧瓶,当反应物温度不再上升而趋下降时,才可继续加混酸。反应温度应保持在40—50℃,若超过50℃,可用冷水浴冷却烧瓶,加料完毕后,把烧瓶放在水浴上加热,约10分钟内把水浴加热到55-60℃,并保持30分钟,间歇地振荡烧瓶。
③冷却后将反应物倒入分液漏斗,静置分层,分出酸液和粗硝基苯,由于工业浓H2SO4中含有少量汞盐等杂质有催化作用,使反应产物中含有苦味酸(2,4,6-三硝基苯酚)和2.4-二硝基苯酚使粗硝基苯呈浅黄色,此外还含有间二硝基苯。已知:苦味酸与2,4-二硝基苯酚均有酸性,能与碱反应;间二硝基苯性质与硝基苯类似。请回答下列问题
(1)步骤①中长颈漏斗的作用
a ,
b 。
(2)步骤 ②中,每加入一次混酸,必须振荡烧瓶的目的 。
(3)步骤②中,需严格控制温度的原因 。
(4)步骤③中,静置分层后,粗硝基苯在分液漏斗 层。
(5)要将粗硝基苯中混有少量酸液、苦味酸、2,4一二硝基苯酚以及二硝基苯,除去得到纯净的硝基苯必须进行的五步操作名称为
a b c d e 。
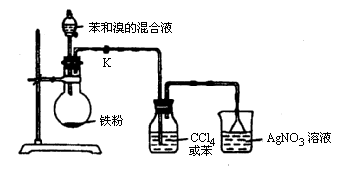
查看习题详情和答案>>实验室用如图所示装置进行苯与溴反应的实验
请回答下列问题
(1)若装置中缺洗气瓶,则烧杯中产生的现象无法说明苯与溴的反应是取代反应,理由是________.
(2)反应后得到的粗溴苯中溶有少量的苯、溴、三溴苯、溴化铁和溴化氢,可通过以下操作除去:①水洗;②碱洗;③水洗;④干燥;⑤…….其中,操作②碱洗的目的是________,完成操作④干燥后,接下来的操作⑤是________(填操作名称).
(3)如果省略(2)中的操作①,一开始就进行碱洗,会对后面的操作造成什么影响?(简要说明理由)________.
查看习题详情和答案>>实验室用下图所示装置进行苯与溴反应的实验请回答下列问题
(1)若装置中缺洗气瓶,则烧杯中产生的现象无法说明苯与溴的反应是取代反应,理由是__________________________________________________________________________
______________________________________________________________________________.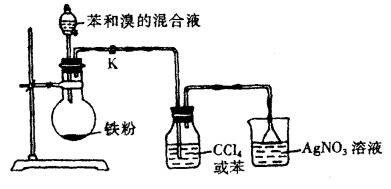
(2)反应后得到的粗溴苯中溶有少量的苯、溴、三溴苯、溴化铁和溴化氢,可通过以下操作除去,①水洗;②碱洗;③水洗;④干燥;⑤…….其中,操作②碱洗的目的是___________ _ __,完成操作④干燥后,接下来的操作⑤是_____________(填操作名称).
(3)如果省略(2)中的操作①,一开始就进行碱洗,会对后面的操作造成什么影响?(简要说明理由)
________________________________________________________________________
查看习题详情和答案>>