网址:http://m.1010jiajiao.com/timu_id_6606[举报]
(一)选择题
1.D 2.C 3.C 4.D 5.C 6.D 7.B、C 8.B 9.C 10.A 11.B 12.C、D 13.C、D 14 .B、C 15.B 16.D 17.D 18.D 19.B 20.C 21.A 22.A、B 23.B 24.D 25.D
(二)非选择题
1.答案为
2.(1)(A)4 (B)7 (C)5 (2)(D)4 (E)4 (F)2
3.(1)N2H4,
(2)H2N-NH2+H2OH2N-NH2?H2O
H2N-NH2?H2O+H2OH2O?H2N-NH2?H2O
4.(1)NxHy+O2N2+H2O (2)N2H4
5.(1)略 (2)14.7 (3)NOx(或NO、NO2)、CO.
6.(1)23.3% (2)1.26×1018kJ (3)A=[×6×44g/mol]÷1000或A= Q为每生成1 mol葡萄糖所需要吸收的能量(或:每消耗6 mol CO2所需吸收的能量)
7.(1)b、c、b、c、b (2)NaOH―CH3CH2OH溶液、加热
(3)
8.(1)甲酸甲酯,HCHO,
(2)CH3COONa+NaOHNa2CO3+CH3↑
(3)(或 ,
9.(1)3∶2∶3 (2)
10.(1)CH2O (2)30,60;CH2O,C2H4O2
14.(1)乙二醇,乙二酸
(2)①,②,④ (3)②,④
(4)
17.(1) 40%
(2)CH3CH2CH2CHO,(CH3)2CHCHO,
(3)CH2=CHCH(CH3)2
18.(1)2ClCH2COO?-2eClCH2CH2Cl+2CO2
2H2O+2eH2+2OH-
(2)
(3)
? ?n
19.(1)CaC2+2H2OCa(OH)2+C2H2↑
(2)CH≡CH+H2CH2=CH2
(3)CH2=CH2+HClCH3CH2Cl
20.(1)n(C)=0.160(mol) n(H)=0.120(mol) n(O)=0.08(mol)
(2)最简式为C4H3O2.
(3)
21.(1)4 (2)C4H6O4 (3)5,
(4)CH3OH, C2H5OH,H2O
22.A:CH―CH3―CH3,B:CH2―CH3―CH2OH,C:CH3CH2―O―CH3;A∶B∶C=1∶3∶6
|
OH
O
‖
23.(1)CH4,CH3―C―CH3
(2)CH2=C―COOH+CH3OHCH2=C―COOCH3+2H2O
| |
CH3 CH3
(3)加成,取代
COOCH3
|
(4)nCH2=C-COOCH3?CH2―C?n
| |
CH3 CH3
24.(1)CxHy+()O2mCO2+H2O+(x-m)CO (2)C4H8
(3)
分子式
n(CO)∶n(CO2)
C3H8
1∶2
C4H6
1∶3
O
‖
25.(1)(略) (2)缩聚nCH3 ―CH―COOHH?O―CH―C?n―OH+(n-1)H2O
| |
OH OH
O
‖
(3)H?O―CH―C?nOH+(n-1)H2OnCH3―CH―COOH
| |
OH OH
26.(1)6CO2+12H2OC6H12O6+6H2O+6O2
(2)C+O2=CO2
CnH2n+2+O2nCO2+(n+1)H2O
CH4+2O2=CO2+2H2O
CH4产生的CO2最小,对环境负面影响最小
27.(1)C9H10O2 (2)4
28.(1)O=C=C=C=O
O O
‖ ‖
(2)C3O2+2HClCl―C―CH2―C―Cl]
O O
‖ ‖
C3O2+2C2H5OHC2H5―C―CH2―C―OCH2
29.(1)C15H13O2F(或C15H13FO2)
30.(1)A,B;C,F;D,E (2)都有18O标记。因为反应中间体在消去一分子H2O 时,有两种可能,而乙氧基(OC2H5)是保留的。
(3)(或答中间体) ,因为这个碳原子连有4个原子团。
31.(1)C6H5―CH―NH―CO―C6H5+H2OC6H5―CH―NH2+C6H5COOH
| |
HO―CH―COOH HO―CH―COOH
(2)α (3)C31H38O11
32.(1)0.125;0.30;0.100;5:12:4
(2)可以;因为该最简式中H原子个数已经饱和,所以最简式即分子式C5H12O4
(3)C(CH2OH)4
33.(1)十肽 (2)4个谷氨酸 (3)3个苯丙氨酸
由三种化合物组成的混合物X,组成它的三种化合物互为同分异构体,经实验测得下列结果:
①分取A、B、C各3g在127℃、1.01×105Pa下汽化,测得其体积均为1640ml.将等质量的A、B、C三种有机物在过量的氧气中燃烧,在标准状况下均生成3.36L CO2和3.6g水.
②实验表明:A、B二种有机物与金属钠反应有H2放出,C与金属钠不反应,实验测得3.6g混合物X与足量金属钠反应完毕后在标准状况下收集到0.56g H2.
③实验表明:A、B均能被氧化剂所氧化,C不被氧化剂所氧化,只有A被氧化的最终产物是羧酸.实验测得3.6g有机混合物X被充分氧化后,分离出2.2g羧酸.试解答:
(1)混合物X中含有哪些有机物?
(2)求混合物X中各组成成分的物质的量之比.
查看习题详情和答案>>(16分)X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16。在适当条件下三种单质两两化合,可发生如右图所示变化。己知l个B分子中含有Z元素的原子个数比C分子中含有Z元素的原子个数少1个。请回答下列问题: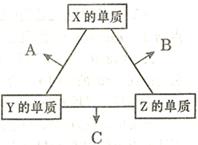
(1)由 X、Y、Z三种元素共同组成的三种不同种类的常见化合物的化学式为 ,相同浓度上述水溶液中由水电离出的c(H+)最小的是 (填写化学式)。
(2)Allis-Chalmers制造公司发现可以用C作为燃料电池的燃料,以氢氧化钾溶液为介质,反应生成对环境无污染的常见物质,试写出该电池负极的电极反应式 ,溶液中OH-向 极移动(填“正”或“负”)。
(3)Z分别与X、Y两元素可以构成18个电子分子甲和乙,其分子中只存在共价单键,常温下甲、乙均为无色液体,甲随着温度升高分解速率加快。
①乙能够将CuO还原为Cu2O,已知每lmol乙参加反应有4mole- 转移,该反应的化学方程式为 。
②将铜粉末用10%甲和3.0mol?L-1H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜的平均溶解速率 (×10-3mol?L-1·min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
_____________________________________________________。
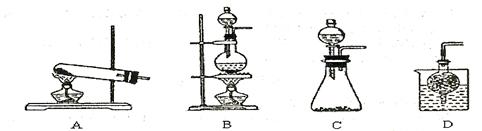
③实验室可用甲作试剂取X的单质,发生装置可选用下图中的 (填装置代号)。
 查看习题详情和答案>>
查看习题详情和答案>>
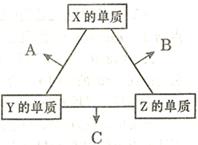
(1)由 X、Y、Z三种元素共同组成的三种不同种类的常见化合物的化学式为 ,相同浓度上述水溶液中由水电离出的c(H+)最小的是 (填写化学式)。
(2)Allis-Chalmers制造公司发现可以用C作为燃料电池的燃料,以氢氧化钾溶液为介质,反应生成对环境无污染的常见物质,试写出该电池负极的电极反应式 ,溶液中OH-向 极移动(填“正”或“负”)。
(3)Z分别与X、Y两元素可以构成18个电子分子甲和乙,其分子中只存在共价单键,常温下甲、乙均为无色液体,甲随着温度升高分解速率加快。
①乙能够将CuO还原为Cu2O,已知每lmol乙参加反应有4mole- 转移,该反应的化学方程式为 。
②将铜粉末用10%甲和3.0mol?L-1H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜的平均溶解速率 (×10-3mol?L-1·min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
_____________________________________________________。
③实验室可用甲作试剂取X的单质,发生装置可选用下图中的 (填装置代号)。
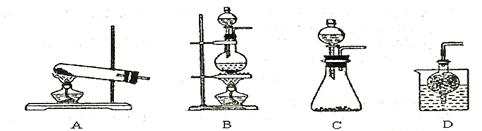
X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,Z分别与X,Y形成B、C两种电子数均等于10的分子且一个B分子中含有的Z原子个数比C分子中少1个请回答下列问题:
(1)Y元素在周期表中的位置是________周期________族.
(2)B的电子式是________,B与C反应的化学方程式为________.
(3)由X、Y、Z形成组成化合物Z4Y2X3的化学键类型是________,其水溶液中各离子浓度大小关系是________
(4)已知Y单质与Z单质生成C的反应是可逆反应,ΔH<0.若X、Z、C的起始浓度分别用a mol/L、b mol/L、c mol/L表示,且a、b、c均不为0,在一定条件下,达到平衡时测得c(Y)=0.5 mol/L、c(Z)=0.3 mol/L、c(C)=1.6 mol/L.则:
①a、b应满足的关系:________
②a的取值范围:________
③将等物质的量的Y、Z两种单质充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应.下列说法正确的有________.
a.达到化学平衡时,正反应速率与逆反应速率相等
b.反应过程中,Y单质的体积分数始终为50%
c.达到化学平衡时,Y、Z两种单质在混合气体中的物质的量之比为1∶1
d.达到化学平衡后,升高温度,C的体积分数减小
甲、乙、丙、丁是由前20号元素组成的物质,以下4种情况下的反应均符合转化关系:甲+乙→丙+丁.请按要求回答下列问题:
(1)若甲和丁是同主族元素组成的单质,且甲的组成元素位于第三周期;乙为水.
①则丙的电子式为________;
②该反应的离子方程式为________.
(2)若甲为固态离子化合物,组成它的两种元素的核电荷数之和为26;乙为水;丙为分于内既含有非极性键又含有极性键的可燃性气体.
①则丙的结构式为________;
②丁的稀溶液与盐酸反应生成1 mol水时放热为X kJ,请写出此反应的热化学方程式________.
(3)若常温下气体甲的水溶液pH大于7;乙为黄绿色气体;丙为无色气体单质,丁为固体铵盐.假设充满甲、乙两种混合气体在集气瓶中恰好完全反应,冷却后再将该集气瓶倒置于水中打开塞子,观察水倒吸入集气瓶中,剩余气体占反应前气体总体积的1/11.
①在甲与乙的反应中,甲具有(填“氧化”或“还原”)________性;
②还可以观察到集气瓶中的现象有________,其中反应的化学方程式为________.
(4)若甲为黄绿色气体单质;乙为固体氧化物,常用作肥料,其水溶液pH<7;丙为氮的氯化物;丁为HCl.当消耗6.72 L Cl2(标准状况下)时得到0.10 mol丙.
①用离子方程式表示乙的水溶液pH<7的原因:________.
②请写出该反应的化学方程式________.