网址:http://m.1010jiajiao.com/timu_id_58282[举报]
研究性学习小组的同学为了了解Cu及其化合物的性质,提出以下问题;
①Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②Fe的+2价化合物的稳定性比+3价化合物的稳定性小,Cu的+l价化合物的稳定性也比+2价化合物的稳定性小吗?
③CuO能被H2,CO等还原,也能被氮的气态氢化物还原吗?
(1)解决问题①需要用到的药品有CuSO4溶液、______(填字母).A.AlCl3溶液B.NaOH溶液 C.稀H2SO4 D.H2O4溶液 假若Cu(OH)2具有两性,应该看到的实验现象是______.
(2)为了比较Cu+l价化合物和+2价化合物的稳定性,他们取Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末氧化亚铜.向氧化亚铜中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在.可以得出的结论是______.根据以上现象写出氧化亚铜和稀硫酸反应的离子方程式______.
(3)为解决问题③,设计了如下的实验装置(夹持装置未画出):
在实验中观察到CuO变成红色物质,无水CuSO4变成蓝色,生成物中还有一种无污染的单质气体Y.现有氮的某种气态氢化物X气体0.0lmol,缓缓通过红热的氧化铜玻璃管完全反应后,测得C装置增重0.36g并收集到单质气体Y0.28g.X气体的摩尔质量______,B中发生反应的化学方程式为______.
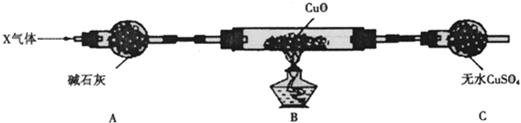
(4)请猜测用上述装置测量时有可能产生误差的原因______(答1条即可)
查看习题详情和答案>>
研究性学习小组的同学为了了解Cu及其化合物的性质,提出以下问题;
①Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②Fe的+2价化合物的稳定性比+3价化合物的稳定性小,Cu的+1价化合物的稳定性也比+2价化合物的稳定性小吗?
③CuO能被H2、CO等还原,也能被NH3还原吗?
(1)解决问题①需要用到的药品有CuSO4溶液、 、 (填字母)。
A.A1Cl3溶液 B.NaOH溶液 C.稀H2SO4 D.H2O2溶液
假若Cu(OH)2具有两性,应该看到的实验现象是 。
(2)为了比较Cu的+1价化合物和+2价化合物的稳定性,他们取98gCu(OH)2固体,加热至800C~1000C时,得到黑色固体粉末,继续加热到10000C以上,黑色粉末全部变成红色粉末X。冷却后称量,X的质量为72g。向X中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在。据此可推得,X的化学式为 ,可以得出的结论是 。
(3)为解决问题③,设计了如下的实验装置(夹持及尾气处理装置未画出):
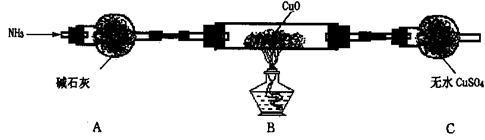
在实验中观察到CuO变成红色物质,无水CuSO4变成蓝色,生成物中还有一种无污染的单质气体。装置A的作用是 ,B中发生反应的化学方程式为 。
查看习题详情和答案>>①Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②Fe的+2价化合物的稳定性比+3价化合物的稳定性小,Cu的+l价化合物的稳定性也比+2价化合物的稳定性小吗?
③CuO能被H2,CO等还原,也能被氮的气态氢化物还原吗?
(1)解决问题①需要用到的药品有CuSO4溶液、 (填字母).A.AlCl3溶液B.NaOH溶液 C.稀H2SO4 D.H2O4溶液 假若Cu(OH)2具有两性,应该看到的实验现象是 .
(2)为了比较Cu+l价化合物和+2价化合物的稳定性,他们取Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末氧化亚铜.向氧化亚铜中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在.可以得出的结论是 .根据以上现象写出氧化亚铜和稀硫酸反应的离子方程式 .
(3)为解决问题③,设计了如下的实验装置(夹持装置未画出):
在实验中观察到CuO变成红色物质,无水CuSO4变成蓝色,生成物中还有一种无污染的单质气体Y.现有氮的某种气态氢化物X气体0.0lmol,缓缓通过红热的氧化铜玻璃管完全反应后,测得C装置增重0.36g并收集到单质气体Y0.28g.X气体的摩尔质量 ,B中发生反应的化学方程式为 .
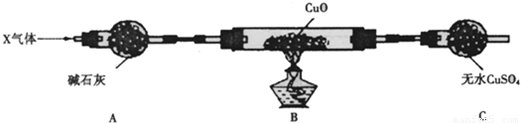
(4)请猜测用上述装置测量时有可能产生误差的原因 (答1条即可) 查看习题详情和答案>>
研究性学习小组的同学为了了解Cu及其化合物的性质,提出以下问题;
①Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②Fe的+2价化合物的稳定性比+3价化合物的稳定性小,Cu的+1价化合物的稳定性也比+2价化合物的稳定性小吗?
③CuO能被H2、CO等还原,也能被NH3还原吗?
(1)解决问题①需要用到的药品有CuSO4溶液、________、________(填字母).
A.A1Cl3溶液
B.NaOH溶液
C.稀H2SO4
D.H2O2溶液
假若Cu(OH)2具有两性,应该看到的实验现象是________.
(2)为了比较Cu的+1价化合物和+2价化合物的稳定性,他们取98 g Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末X.冷却后称量,X的质量为72 g.向X中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在.据此可推得,X的化学式为________,可以得出的结论是________.
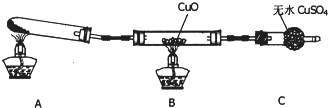
(3)为解决问题③,设计了如下的实验装置(夹持及尾气处理装置未画出):

在实验中观察到CuO变成红色物质,无水CuSO4变成蓝色,生成物中还有一种无污染的单质气体.装置A的作用是________,B中发生反应的化学方程式为________.
I.NH3性质的探究
(1)实验室制取氨气的化学方程式为
(2)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气.你认为他能否达到目的?
(3)该小组的同学设计了如图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性:
①该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是
②利用改进后的装置进行实验,观察到B装置中CuO变为红色物质,C装置中无水CuSO4变为蓝色,同时生成一种无污染的气体.写出氨气与CuO反应的化学方程式
③有同学认为:NH3与CuO反应生成的红色物质中可能含有红色的Cu20.
已知:Cu20是一种碱性氧化物,在酸性溶液中Cu+
| H+ |
Ⅱ.NO2性质的探究
该小组的同学还设计了如图所示装置用以制取NO2并验证NO2能否支持木条燃烧(忽略N2O4的存在,图中铁架台等夹持仪器均已略去).已知:硝酸铜加热分解的化学方程式为2Cu(NO3)2═2CuO+4NO2↑+O2↑
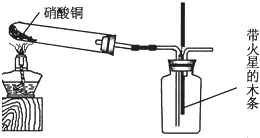
(4)当集气瓶中充满红棕色气体时,带火星的木条复燃了,有的词学得出“N02能支持木条的燃烧”的结论.你认为这一结论是否正确?